高分子材料W的结构简式为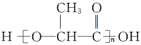 ,有关W的信息如下,据此回答下列问题:
,有关W的信息如下,据此回答下列问题:
(1)葡萄糖的分子式为____ ____,其所含官能团的名称为________________。
(2)反应①的类型为_____ ___。
(3)反应⑥的化学方程式为______________ _______。
(4)B分子有多种同分异构体,其中X的核磁共振氢谱如下图所示: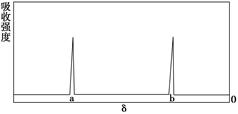
则X的结构简式可能为
____________ ______ ____。
实验室鉴别X可使用___________ _____试剂。
(5)指出W这种高分子材料的一种优点
_____________________ ___ ______ .
X、Y、Z、W是短周期的四种元素,有关他们的信息如下表所示。
| 元素 |
部分结构知识 |
部分性质 |
| X |
X的单质由双原子分子构成,分子中有14个电子 |
X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y |
Y原子的次外层电子数等于最外层电子数的一半 |
Y能形成多种气态氢化物 |
| Z |
Z原子的最外层电子数多于4 |
Z元素的最高正化合价与最低负化合价代数和等于6 |
| W |
W原子的最外层电子数等于2n-3(n为原子核外电子层数) |
化学反应中W原子易失去最外层电子形成Wn+ |
填写下列空白:(提示:不能用字母X、Y、Z、W作答)
(1)Z元素在周期表中的位置是__________;Y的一种氧化物能导致温室效应,该氧化物的电子式为____;Z的单质与W的单质一定条件下可发生反应生成化合物A,A中所含化学键类型为_______。
(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是_______。
(3)实验室制取Z单质的化学方程式为_____________________________。
(4)实验室制取X的氢化物的化学方程式为_____________________________;工业上用此氢化物制取X的最高价含氧酸的第一步反应方程式为__________________________________。
(5)实验室用X的氢化物的水溶液制取W的氢氧化物的离子方程式为_________________。
某溶液X含有H+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行实验,实验内容和相关数据(气体体积在标准状况下测定)如下:
(1)通过上述实验过程,一定不存在的离子是________________________。
(2)写出有关离子方程式:步骤①中生成A________________________。
(3)若测得X溶液中c(H+)="5" mol·L-1,则X溶液中_______(填“含”或“不含”)Fe3+,c(Fe3+)=______mol·L-1(若填不含,则不需计算),X溶液中c(C1-)=____________ mol·L-1。
随着原子序数的递增,八种短周期元素原子半径的相对大小和最高正价或最低负价如图所示。
(1)元素Z位于元素周期表的第__________周期___________族,X与Z可形成18电子的化合物,该化合物的电子式为_______________。
(2)非金属性:Y___________(填“>”“<”或“=”)D。
(3)单质F与EDX溶液反应的化学化学方程式为____________________。
(4)G和H可形成一种化合物,其相对分子质量在90~110之间。且G的质量分数约为31.1%,该化合物的化学式为_________。
光刻胶是一种应用广泛的光敏材料,其合成路线如下(部分试剂和产物略去):
已知:
Ⅰ. (R,R’为烃基或氢)
(R,R’为烃基或氢)
Ⅱ. (R,R’为烃基)
(R,R’为烃基)
(1)A分子中含氧官能团名称为 。
(2)C物质可发生的反应类型为 (填字母序号)。
a.加聚反应 b. 酯化反应 c.还原反应 d.缩聚反应
(3)B与Ag(NH3)2OH反应的化学方程式为 。
(4)乙炔和羧酸X加成生成E,E的核磁共振氢谱为三组峰,且峰面积比为3:2:1,E能发生水解反应,则E的结构简式为 。
(5)与C具有相同官能团且含有苯环的同分异构体有 种,写出其中的一种同分异构体的结构简式为 。
(6)D和G反应生成光刻胶的化学方程式为 。
X、Y、Z、W为电子数相同的分子或离子。X有5个原子核。通常状况下,W为无色液体。它们之间转化关系如下图所示: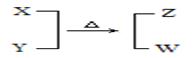
请回答:
(1)Z的电子式是 。
(2)实验室制取Z的的化学方程式: 。
(3)某化学小组同学模拟工业生产制取HNO3,设计下图所示装置,其中a为一个可持续鼓入空气的橡皮球。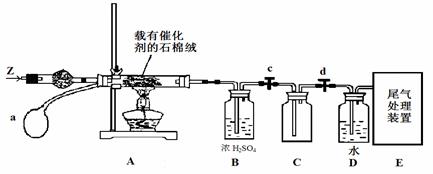
① A中发生反应的化学方程式是 。
② B中浓H2SO4的作用是 。
(4)写出D装置中反应的化学方程式 。