已知有机化合物 A、B、C、D、E存在下图所示转化关系,且C能跟NaHCO3发生反应,C和D的相对分子质量相等,E为无支链的化合物。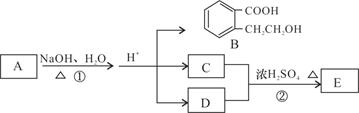
请回答下列问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为 。
(2)B在一定条件下可以发生缩聚反应生成某高分子化合物,此高分子化合物的结构简式为 。
(3)C的核磁共振氢谱中有 个峰;D也可以由卤代烃F在NaOH溶液中加热来制取,写出此反应的化学方程式 。
(4)A的结构简式是 。
(5)B有多种同分异构体,请写出一种同时符合下列四个条件的结构简式: 。
a.能够发生水解 b.能发生银镜反应
c.能够与FeCl3溶液显紫色 d.苯环上的一氯代物只有一种
在 K2Cr2O7 + 14HCl ="===" 2KCl + 2CrCl3 + 3Cl2›+ 7H2O反应中。
="===" 2KCl + 2CrCl3 + 3Cl2›+ 7H2O反应中。
(1) 元素被氧化, 是氧化剂,氧化产物是 ;
(2)此反应若转移了12mol的电子,则生成氯气 L(标准状况)
⑴钾和硝酸钾反应可制得氧化钾K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有___________g
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。请尝试写出超氧化钾与二氧化碳反应的化学方程式
__________________________________________________________________________,为了维持气压稳定可以使用超氧化钾和过氧化钾的混合物使吸收的CO2与生成的O2体积相同(同温同压),则它们的物质的量之比为____________
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比。如果产物A只含有两种化合物,写出所有可能的化学式并计算A中两种化合物的物质的量之比。
(一)补全以下检验混合物中存在K2CO3的实验步骤及相关现象
1.取混合物样品溶于水,分别取少量溶液进行以下实验
2._________________________________________则一定存在K+;
3.___________________________________________________则一定存在CO32—。
(二)测定K2CO3质量分数
(1)甲同学用图1所示装置,把xg的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时检查该装置气密性的方法是
。
(2)乙同学用图2代替图1中的收集装置,则所测K2CO3质量分数(填“偏大”、“偏小”、“不变”),你的改进方案是。
(3)丙同学用图3装置测定CO2的质量,该装置存在较多缺陷,从而导致实验误差,请你填写其中的三点缺陷:I;
Ⅱ
Ⅲ

(1)试剂(a)是________________,(b)是______________,(c)是____________;
(2)分离方法①是________________,③是____________________;进行上述操作要用到的玻璃仪器有_______________________________。
(3)按上述操作,不考虑损耗,在理论上158g明矾(摩尔质量474g/mol)最多可以制得硫酸铝晶体〔Al2(SO4)3•18H2O〕(摩尔质量666g/mol) _____g,至少可以制备K2SO4(摩尔质量174g/mol)_______g。
(1)该反应中,被氧化的元素是____________,氧化剂是____________。
(2)写出该反应的化学方程式并标明电子转移的方向和数目:
___________________________________________________________________________。