下列画有横线的反应物在反应中不能完全消耗的是( )
| A.将含有少量CO2的CO通入足量Na2O2的试管中并不断用电火花引燃 |
| B.向等物质的量的干冰和CaO的混合物中加几滴水 |
| C.将1molCu置于含2molH2SO4的浓溶液中加热 |
| D.在强光持续照射下,向过量的Ca(ClO)2浊液中通入少量的CO2 |
电子层数相同的短周期元素X、Y、Z、W,其中X的最外层电子数比K层少1,Y的最外层电子数比K层多l,Z的单质常用于制造太阳能电池,w的原子半径是同周期中最小的。下列推断中正确的是()
| A.Z的氢化物的热稳定性强于w的氢化物 |
| B.z的氧化物与水反应可制得相应的含氧酸 |
| C.X、Y、W的原子半径依次减小,对应的离子半径依次增大 |
| D.X、Y、W的最高价氧化物对应水化物之间互相都能发生反应 |
Li—SO2电池具有输出功率高和低温性能好等特点,其电解质是LiBr,溶剂是碳酸丙烯酯和乙睛,电池反应为2Li+2SO2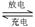 Li2S2O4。下列说法正确的是()
Li2S2O4。下列说法正确的是()
| A.该电池反应为可逆反应 |
| B.放电时,Li+向负极移动 |
| C.充电时,阴极反应式为Li++e-===Li |
| D.该电池的电解质溶液可以换成LiBr的水溶液 |
盖斯定律认为能量总是守恒的,化学反应过程一步完成或分步完成,整个过程的热效应是相同的。
己知:①H2O(g)=====H2O(l)△H1===Q1kJ·mol-1
②C 2H 5OH(g)====C2H 5OH(l)△H2="===Q" 2 kJ·mol-1
③C 2 H 5 OH(g)+3O2(g)——2CO2(g)+3 H 2 O(g)△H3====Q 3 kJ·mol-1
若使23g液态酒精完全燃烧,最后恢复到室温,则放出的热量为(kJ)
| A.Q1+Q2+Q3 | B.1.5Q1-0.5Q2+0.5Q3 |
| C.0.5Q1-1.5Q2+0.5Q3 | D.0.5(Q1+Q2+Q3) |
下列关于有机物的说法中,不正确的是()
| A.糖类、油脂和蛋白质在一定条件下都能发生水解反应 |
| B.2,5一二甲基己烷的核磁共振氢谱中会出现三组峰 |
| C.甲烷、苯、乙醇和乙酸在一定条件下都能发生取代反应 |
| D.分子式为C5H12的有机物只有三种,它们属于同分异构体 |
下述实验不能达到预期目的的是()
| 编号 |
实验内容 |
实验目的 |
| A |
将SO2通入酸性KMnO4溶液中 |
证明SO2具有漂白性 |
| B |
将Cl2通入NaBr溶液中,然后加入CCl4,振荡、静置 |
比较氯与溴的氧化性强弱 |
| C |
将铜片分别与浓、稀硝酸反应 |
探究浓、稀硝酸氧化性的相对强弱 |
| D |
向盛有20g蔗糖的烧杯中加入几滴水,搅拌均匀。再加入少许浓硫酸,迅速搅拌。 |
探究浓硫酸的脱水性 |