已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如下图所示,下列说法中不正确的是( )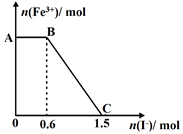
| A.图中AB段的氧化剂为K2Cr2O7 |
| B.图中BC段发生的反应为2Fe3++2I- =2Fe2++I2 |
| C.开始加入的K2Cr2O7为0.25 mol |
| D.K2Cr2O7可与FeSO4反应的物质的量为1:3。 |
氢氧燃料电池是将H2和O2分别通入电池,穿过浸入20%—40%的KOH溶液的多孔碳电极,其电极反应式为H2+2OH--2e- 2H2O和
2H2O和 O2+H2O+2e-
O2+H2O+2e- 2OH-,则下列叙述正确的是()
2OH-,则下列叙述正确的是()
| A.通入H2的一极是正极,通入O2的一极是负极 |
| B.通入O2的一极是正极,通入H2的一极是负极 |
| C.工作一段时间后电解质溶液的pH增大 |
| D.工作时负极区附近pH增大 |
一定条件下,在2SO2+O2  2SO3的化学平衡体系中,各物质的浓度分别是:SO2:2mol/L,O2 : 0.8mol/L,SO3 : 2.4mol/L,则氧气在起始时的浓度可能是()
2SO3的化学平衡体系中,各物质的浓度分别是:SO2:2mol/L,O2 : 0.8mol/L,SO3 : 2.4mol/L,则氧气在起始时的浓度可能是()
| A.0.8—2mol/L | B.0—2mol/L | C.0—0.8mol/L | D.无法确定 |
已知:C(s)+CO2(g) 2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是()
2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是()
| A.升高温度和减小压强 | B.降低温度和减小压强 |
| C.降低温度和增大压强 | D.升高温度和增大压强 |
如图1所示,可逆反应:mA(g)+nB(g) xC(g),在不同温度、压强下反应物A的转化率的变化情况。下列对于反应的热效应和反应方程式中A、B、C的系数的判断中,正确的是()
xC(g),在不同温度、压强下反应物A的转化率的变化情况。下列对于反应的热效应和反应方程式中A、B、C的系数的判断中,正确的是()
A.放热,m+n>x
B.放热,m+n<x
C.吸热,m+n<x
D.吸热,m+n>x
在恒温、恒容的条件下,有反应2A(g)+2B(g) C(g)+3D(g),现从两条途径分别建立平衡。途径I:A、B的起始浓度为2mol·L—1;途径II:C、D的起始浓度分别为2mol·L—和6mol·L—;则以下叙述正确的是()
C(g)+3D(g),现从两条途径分别建立平衡。途径I:A、B的起始浓度为2mol·L—1;途径II:C、D的起始浓度分别为2mol·L—和6mol·L—;则以下叙述正确的是()
A.两途径最终到平衡时,体系内混合气的百分组成相同
B.两途径最终达到平衡时,体系内混合气的百分组成不同
C.达平衡时,途径I的反应速率v(A)等于途径II的反应速率v(A)
D.达平衡时,途径I所得混合气的密度为途径II所得混合气密度的1/2