根据下图海水综合利用的工业流程图,判断下列说法正确的是( )
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
| A.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| B.在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
| D.从第③步到第⑤步的目的是为了浓缩 |
化学工作者从下面的有机反应RH+Cl2(g)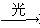 RCl(l)+HCl(g)受到启发提出的在农药和有机合成工业中可获得副产品HCl的设想已成为现实,试指出由上述反应产物分离得盐酸的最佳方法是( )
RCl(l)+HCl(g)受到启发提出的在农药和有机合成工业中可获得副产品HCl的设想已成为现实,试指出由上述反应产物分离得盐酸的最佳方法是( )
| A.水洗分液法 | B.蒸馏法 | C.升华法 | D.有机溶剂萃取法 |
下列实验方案不合理的是( )
| A.鉴定蔗糖水解产物中有葡萄糖:直接在水解液中加入新制Cu(OH)2悬浊液 |
| B.鉴别织物成分是真丝还是人造丝:用灼烧的方法 |
| C.鉴定苯中无碳碳双键:加入高锰酸钾酸性溶液 |
| D.鉴别己烯和苯:将溴的四氯化碳溶液分别滴加到少量己烯和苯中 |
市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣服上的汗渍、血迹及人体排放的蛋白质、油脂遇到它都能水解而除去。下列衣料中不能用加酶洗衣粉洗涤的是( )
①棉织品 ②毛织品 ③腈纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥锦纶织品
| A.①②③ | B.②④ | C.③④⑤ | D.③⑤⑥ |
加拿大阿尔贡天文台在星际空间发现了HC9N链状分子,其结构式为HC≡C—C≡C—C≡C—C≡C—C≡N,这是人类迄今发现的最重星际有机分子,有关该分子的说法不正确的是( )
| A.该物质属于不饱和烃 |
| B.该分子属于有机化合物 |
| C.该分子在一定条件下可发生加成反应 |
| D.该分子碳、氮原子均满足8电子结构 |
以下有关物质结构的描述正确的是( )
| A.甲苯分子中的所有原子可能共平面 |
| B.苯乙烯分子中的所有原子可能共平面 |
| C.二氯甲烷分子为正四面体结构 |
| D.乙烷分子中的所有原子不可能都在同一平面内 |