以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
回答下列问题:
Ⅰ、(1)在一定条件下,SO2转化为SO3的化学反应为2SO2(g)+O2(g)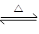 2SO3(g),该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为 。
2SO3(g),该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为 。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是 、 。
(3)通氯气氧化时,发生的主要反应的离子方程式为 ;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为 (写化学式)。
Ⅱ、 已知: CuCl2溶液中含有少量杂质FeCl2,为制备纯净的CuCl2·2H2O晶体,拟定实验步骤如图所示: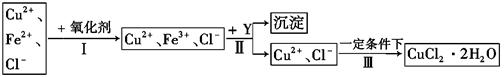
请回答下列问题:
(4)步骤Ⅰ中,将Fe2+转化为Fe3+最好选用下列氧化剂中的 (填字母)。
A.K2Cr2O7 B.NaClO C.H2O2
该反应的离子方程式为 。
(5)在步骤Ⅱ中,加入Y的目的是为了调节溶液的酸度以促使Fe3+沉淀完全,Y可以是下列物质中的 (填字母)。
A.NaOH B.Cu C.Cu2(OH)2CO3
(6)步骤Ⅲ应控制的实验条件是 。
已知A(g)+B(g) C(g)+D(g);△H="a" kJ/mol。反应过程中能量变化如图所示,E为反应发生所需要的能量。回答下列问题。
C(g)+D(g);△H="a" kJ/mol。反应过程中能量变化如图所示,E为反应发生所需要的能量。回答下列问题。
(1)该反应的△H0(选填“>”“<”)。当反应达到平衡时,升高温度,A的转化率(选填“增大”“减小”“不变”)。
(2)在某温度下,反应物的起始浓度分别为:c(A)=1mol/L,c(B)=2.4mol/L。达到平衡后,A的物质的量浓度为0.4mol/L,此时B的转化率为。
(3)一定条件下,向体积为2 L的恒容密闭容器中充入l mol A(g)和3 mol B(g),判断该反应达到平衡状态的依据是(填序号)。
①c(A)=c(C)
②容器内压强不变
③混合气体的平均相对分子质量不变
④v(逆)(D)=v(正)B
(4)在反应体系中加入催化剂后反应速率增大,反应发生所需要的能量E1E(选填“>”“<”“=”),这是因为;△H(选填“增大”“减小”“不变”),这是因为。
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是
(用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的。
a.NH3 b.CO2 c.NaOH d.HNO3
② 以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为。取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是
以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为。取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是
。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不有石墨作阳极的原因是。
(3)利用右图装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于处。若X为锌,开关K置于M处,该电化学防护法称为。
某化学反应2A  B + D在不同条件下进行,B、D的起始浓度为0,把反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示。
B + D在不同条件下进行,B、D的起始浓度为0,把反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示。 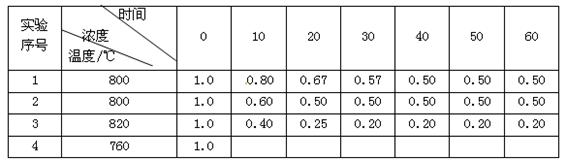
根据上述数据,回答下列问题:
(1)在实验1中,0~10min内的反应速率v(A)为 mol•L -1••min -1。
(2)与实验1相比,实验2的反应速率更 (填"快"或"慢"),其原因可能是 。
(3)根据实验1和实验3的数据分析升温对该反应的影响,写出两条结论:① ;
② 。
(4)实验4只改变温度,其它条件不变。请在答题卡的相应位置画出实验1和实验4的"浓度-时间"关系曲线。 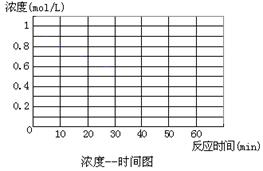
阻垢剂可防止工业用水过程中无机物沉积结构,经由下列反应路线可得知到E和R两种阻垢剂(部分反应条件略去)
(1)阻垢剂E的制备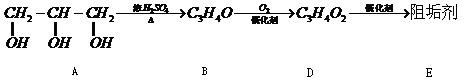
①A可由人类重要的营养物质
 水解制得(填“糖类”、“油脂”或“蛋白质”)
水解制得(填“糖类”、“油脂”或“蛋白质”)
②B与新制的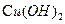 反应生成D,其化学方程式为。
反应生成D,其化学方程式为。
③D经加聚反应生成E,E的结构简式为。
(2)阻垢剂R的制备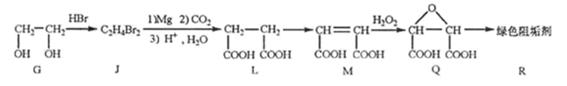
①G→J为取代反应,J的结构简式为。
②由L制备M的反应步骤依次为: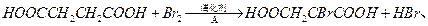
、(用化学方程式表示)。
③1mol Q的同分异构体T(碳链无支链)与足量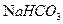 溶液作用产生2mol
溶液作用产生2mol 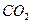 ,T的结构简式为(只写一种)。
,T的结构简式为(只写一种)。
(8分)化合物A含硫(每个分子只含一个硫原子)、氧以及一种或几种卤素。少量A与水反应完全水解但不发生氧化或还原反应,所有反应产物均可溶于水。将A配成水溶液稀释后分成几份,分别加入一系列0.1mol/L的试剂,现象如下:
①加入硝酸酸化的硝酸银,产生白色沉淀;
②加入氯化钡溶液,无沉淀产生;
③溶液经酸化后加入高锰酸钾溶液,紫色褪去,再加入硝酸钡溶液,产生白色沉淀。
⑴由①判断组成该化合物的元素中,肯定存在的卤素有,由②判断A与水反应后生成的溶液中肯定不存在的离子有 。由③判断A与水反应后生成的溶液中肯定存在的离子有 .
。由③判断A与水反应后生成的溶液中肯定存在的离子有 .
⑵要确定该化合物的分子式,称取11.90gA溶于水稀释至250.00mL,取25.00mL溶液加入足量的高锰酸钾和硝酸钡溶液,使沉淀完全,沉淀经洗涤、干燥后称重为2.33g。试确定A的化学式,写出计算推理过程。