(8分)U、W、X、Y、Z都是短周期元素,且原子序数依次增大。其中U与W可形成三角锥形分子甲,U与X可形成常温下呈液态的分子乙,甲、乙均为10 电子分子;Y 元素原子的 K 层电子数与M层电子数相同;Z元素的单质、氧化物均为原子晶体。请回答下列问题:
(1) Z元素在周期表中的位置 。
(2)X、Y、Z三种元素的原子半径由小到大的顺序是 (用元素符号表示)。
(3)U与X形成的18电子化合物的电子式是 。
(4) ZX2与NaOH溶液反应的化学方程式是 。
(5)已知:① N2(g) + 3H2 (g)= 2NH3 (g) △H=-92.4kJ/mol
②2H2(g) + O2(g) = 2H2O(g) △H=-483.6kJ/mol
试写出氨气完全燃烧生成气态水的热化学方程式 。
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g)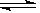 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)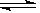 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)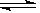 SO3(g)+NO(g)的ΔH=kJ·mol-1。
SO3(g)+NO(g)的ΔH=kJ·mol-1。
(2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=。(保留2位小数)
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)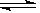 CH3OH(g)。
CH3OH(g)。
CO在不同温度下的平衡转化率与压强的关系如图所示。
该反应ΔH0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是。
25℃时,①醋酸②次氯酸③氢氟酸的电离常数分别是1.8×10-5、3.0×10-8、3.5×10-4。请推测:
(1)它们的酸性由强到弱的顺序为______________________(填序号,下同),
(2)相同浓度的溶液中,氢离子浓度最大的是___________;
(3)氢离子浓度相同的溶液中,酸的浓度最大的是。
把煤作为燃料可以通过下列两种途径:
途径I:C(s)+O2(g) CO2(g) ΔH=E1 ①
CO2(g) ΔH=E1 ①
途径II:先制水煤气:C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②
再燃烧水煤气:H2(g)+1/2O2(g) H2O(g) ΔH=E3③
H2O(g) ΔH=E3③
CO(g)+1/2O2(g) CO2(g) ΔH=E4④ ,试回答下列问题:
CO2(g) ΔH=E4④ ,试回答下列问题:
(1)判断两种途径放热:途径I放出的热量 _____(填“大于”、“等于”、“小于”)途径II放出的热量。
_____(填“大于”、“等于”、“小于”)途径II放出的热量。
(2)E1、E2、E3、E4的数学关系式 是_____________________________________。
是_____________________________________。
(3)由于制取水煤气反应里,反应物所具有的总能量_______(填“大于”、“等于”、“小于”)生成物所具有的总能量,正反应又是熵增加的反应,为了让该反应自发进行,要使反应条件为_______。
苯乙烯是一种重要的化工合成原料。现由苯乙烯合成聚三溴代苯乙烯和另外一种高聚物M的工艺如下:
已知:苯环上的取代反应有如下定位规律:当苯环上已经有了一个取代基时,新引进的取代基因受原取代基的影响而取代其邻、对位或间位的氢原子。使新取代基进入它的邻、对位的取 代基有—R(烷基)、—NH2等;使新取代基进入间位的取代基有—COOH、—NO2等;
代基有—R(烷基)、—NH2等;使新取代基进入间位的取代基有—COOH、—NO2等;
(1)D是高分子化合物,写出D的结构简式______________。
(2)①②③④⑤反应中属于取代反应的是________;
反应⑧的类型为________ 。
(3)设计反应①、③的目的是_______
(4)写出下列反应的化学方程式
反应③:________
反应⑦:________
(5)G有多种同分异构体,写出任意一个符合下列条件的同分异构体的结构简式________ 。
①能发生银镜反应;②能与FeCl3溶液发生显色反应;
③核磁共振谱氢图中出现6组吸收峰。
工业上合成氨的反应是:N2(g)+3H2(g)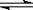 2NH3(g) ΔH=-92.20 kJ·mol-1。
2NH3(g) ΔH=-92.20 kJ·mol-1。
(1)下列事实中,不能说明上述可逆反应已达到平衡的是________
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成n mol N—H的同时生成n mol N≡N
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1︰3︰2
④N2、H2、NH3的体积分数不再改变
⑤混合气体的平均摩尔质量不再改变
⑥混合气体的总物质的量不再改变
(2)已知合成氨反应在某温度下2L的密闭容器中进行,测得如下数据:
| 时间(h) 物质的量(mol) |
0 |
1 |
2 |
3 |
4 |
| N2 |
1.50 |
n1 |
1.20 |
n3 |
1.00 |
| H2 |
4.50 |
4.20 |
3.60 |
n4 |
3.00 |
| NH3 |
0 |
0.20 |
N2 |
1.00 |
1.00 |
根据表中数据计算:
①反应进行到2小时时放出的热量为________
②0~1小时内N2的平均反应速率________ mol·L-1·h-1;
③此条件下该反应的化学平衡常数K="" ________(保留两位小数)
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00mol,化学平衡将向________方向移动(填“正反应”或“逆反应”、“不移动”)。