下列说法错误的是
| A.石油分馏时温度计水银球位置处在蒸馏烧瓶的支管口附近 |
| B.5mL 10%硫酸铜溶液中滴入5滴5%氢氧化钠溶液,再加入1mL葡萄糖溶液,加热,可观察到砖红色沉淀 |
| C.在乙醇中加入钠可产生氢气 |
| D.浓HNO3应保存在棕色试剂瓶中,并贮存在避光、低温处 |
向体积为Va的0.05 mol·L-1 CH3COOH溶液中加入体积为Vb的0.05 mol·L-1 KOH溶液,下列关系错误的是()
| A.Va>Vb时:c(CH3COOH)+c(CH3COO-)>c(K+) |
| B.Va = Vb时:c(CH3COOH)+c(H+) = c(OH-) |
| C.Va<Vb时:c(CH3COO-)>c(K+)>c(OH-)>c(H+) |
| D.Va与Vb任意比时:c(K+)+c(H+) = c(OH-)+c(CH3COO-) |
在一定条件下,可逆反应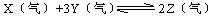 ,达到平衡时有50%的Y转化为Z,若此时X的转化率为25%,则起始充入容器的X与Y物质的量之比应为
,达到平衡时有50%的Y转化为Z,若此时X的转化率为25%,则起始充入容器的X与Y物质的量之比应为
()
| A.3∶2 | B.1∶2 | C.2∶3 | D.1∶3 |
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,其工作原理如下图所示。下列关于固体燃料电池的有关说法正确的是()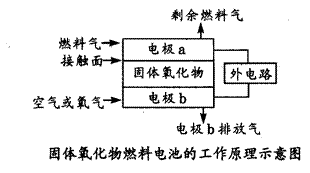
A.电极b为电池负极,电极反应式为:O2+4e-=2O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,接触面上发生的反应为:H2+2OH--2e-= 2H2O
D.若C2H4作为燃料气,接触面上发生的反应为:C2H4+6O2--12e-= 2CO2+2H2O
右图是698K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是()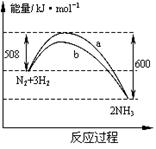
A.该反应的热化学方程式为:N2+3H2 2NH3△H=-92kJ·mol-1 2NH3△H=-92kJ·mol-1 |
| B.b曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热改变 |
| D.温度、体积一定,通入1molN2和3molH2反应后放出的热量为Q1kJ,若通入2 molN2 |
和6 molH2反应后放出的热量为Q2kJ则184>Q2>2Q1
下列离子方程式书写正确的是()
| A.锌粒溶于醋酸溶液: Zn + 2CH3COOH = Zn2+ + 2CH3COO-+ H2↑ |
| B.石灰水与足量的小苏打溶液混合: Ca2++OH-+HCO  =CaCO3↓+H2O =CaCO3↓+H2O |
| C.SO2气体通入到硝酸钡溶液中: Ba2++SO2+H2O=BaSO3↓+2H+ |
| D.AlCl3溶液加入NaAlO2溶液: |
Al3++3AlO +3H2O=4Al(OH)3↓
+3H2O=4Al(OH)3↓