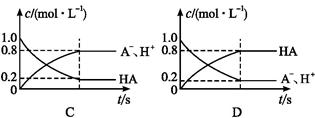
一元弱酸HA(aq)中存在下列电离平衡:HA A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )
A-+H+。将1.0 mol HA分子加入水中制得1.0 L溶液,下图中,表示溶液中HA、H+、A-的物质的量浓度随时间而变化的曲线正确的是( )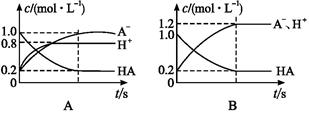
能用H++OH-=H2O来表示的化学反应是
| A.氢氧化镁和稀盐酸反应 | B.Ba(OH)2溶液滴入稀硫酸中 |
| C.澄清石灰水和稀硝酸反应 | D.二氧化碳通入澄清石灰水中 |
下列分散系最稳定的是
| A.悬浊液 | B.乳浊液 | C.胶体 | D.溶液 |
选择萃取剂将碘水中的碘萃取出来,这中萃取剂应具备的性质是
| A.不溶于水,且必须易与碘发生化学反应 | B.不溶于水,且比水更容易使碘溶解 |
| C.不溶于水,且必须比水密度大 | D.不溶于水,且必须比水密度小 |
已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是
| A.KClO3是氧化剂 |
| B.被氧化与被还原的氯元素的质量比为5:1 |
| C.H2SO4既不是氧化剂又不是还原剂 |
| D.1mol KClO3参加反应时有10mol电子转移 |
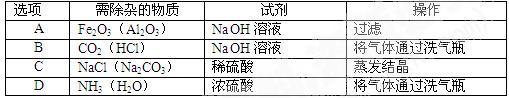
除去下列括号内的杂质,所加试剂和操作均正确的是