某一反应物的浓度是2.0 mol·L-1,经过4 min后,它的浓度变成1.68 mol·L-1,则在这4 min内它的平均反应速率为( )
| A.0.2 mol·L-1·min-1 |
| B.0.1 mol·L-1·min-1 |
| C.0.04 mol·L-1·min-1 |
| D.0.08 mol·L-1·min-1 |
下列实验基本操作(或注意事项)中,主要是从实验安全考虑的是( )
| A.实验剩余的药品一般不能放回原试剂瓶 |
| B.可燃性气体的验纯 |
| C.气体实验装置在实验前进行气密性检查 |
| D.滴管不能交叉使用 |
在盛放浓硫酸的试剂瓶上应印有如下图所示警示标记中的( )
向100 mL0.1 mol/L硫酸铝铵[NH4A1(SO4)2]溶液中逐滴滴入0.1mol·L-lBa(OH)2溶液。随着Ba(OH)2溶渡体积V(横坐标)的变化,沉淀总物质的量n(纵坐标)的变化如图所示。则下列说法中正确的是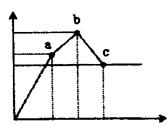
| A.a点的溶液呈中性 |
| B.c点溶液呈碱性 |
| C.c点加入Ba(OH)2溶液的体积为200 mL |
| D.b点发生反应的离子方程式是:A13++2SO42-+2Ba2++3OH-==A1(OH)3↓+2BaSO4↓ |
某溶液中只可能含有下列离子中的几种(不考虑溶液中含的较少的H+和OH-)Na+、NH4+、SO42-、CO32-、NO3-。取200mL该溶液,分为等体积的二份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL。实验2:第二份先加入足量的盐酸,无现象,再加足量的BaCl2溶液,得固体2.33克。下列说法正确的是
| A.该溶液中可能含有Na+ |
| B.该溶液中肯定含有NH4+、SO42-、CO32-、NO3- |
| C.该溶液中一定不含NO3- |
| D.该溶液中一定含Na+,且c(Na+)≥0.1mol/L |
向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入c mol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系正确的是
| A.c=l000b/(22.4V) | B.5m/6<p<17m/9 |
| C.n=m+17Vc | D.p=m+Vc/125 |