下列离子方程式书写正确的是
| A.向水中通入氯气:Cl2+H2O=2H++Cl-+ClO- |
| B.向氯化铁溶液中加入铜:2Fe3++3Cu=2Fe+3Cu2+ |
| C.将含等物质的量的NaHCO3和Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| D.镁和稀硝酸反应:Mg+2H+= Mg2++H2↑ |
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是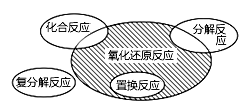
| A.Cl2+2KBr =Br2+2KCl |
B.2NaHCO3 Na2CO3+H2O+CO2↑ Na2CO3+H2O+CO2↑ |
| C.4NO2+O2+2H2O =4HNO3 |
| D.2Na2O2+2CO2=2Na2CO3+O2 |
认真研读课本是一种良好的学习习惯、按照课本所述,下列说法不正确的是
| A.检验试样时,不能将检测试剂一次加入全部待检测试样中 |
| B.在能源丰富而淡水短缺的国家,常利用蒸馏法大规模淡化海水 |
| C.按照分散质或分散剂状态的不同,可以把分散系分为溶液、胶体和浊液三种 |
| D.在相同的温度和压强下,任何气体粒子之间的距离可以看成是相等的 |
储存和运输氢氧化钠的容器上应张贴的图标是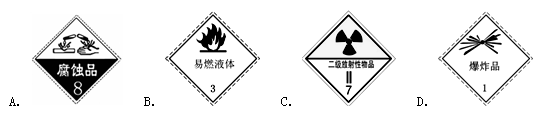
常温,下列各组离子在指定溶液中能大量共存的是
| A.pH=1的溶液中:I-、NO3-、SO42-、Na+ |
| B.由水电离的c(H+)=1×10-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
、下列图示与对应的叙述相符的是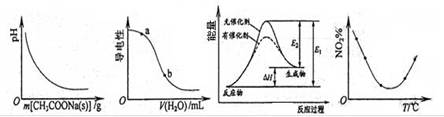
| A.图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 |
| B.图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |
| C.图丙表示催化剂能改变化学反应的焓变 |
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应: ,相同时间后测得NO2含量的曲线,则该反应的△H<0 ,相同时间后测得NO2含量的曲线,则该反应的△H<0 |