单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法正确的是( )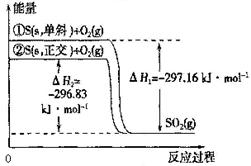
| A.S(s,单斜) = S(s,正交)△H =" +" 0.33 kJ·mol-1 |
| B.相同物质的量的正交硫比单斜硫所含有的能量高 |
| C.正交硫比单斜硫稳定 |
| D.①表示断裂1mol O2中的共价键所吸收的能量比形成l mol SO2中的共价键所放出的能量少297.16 kJ |
阻断病毒附着于敏感细胞的金刚乙胺,对于多种甲型流感病毒都具很好的抑制作用,金刚乙胺可由金刚烷制得。1-溴金刚烷的结构如图所示,若它与NaOH醇溶液反应后所得物质的同分异构体中,含有苯环且只有一个取代基的同分异构体有:
| A.5种 | B.4种 | C.3种 | D.2种 |
下列化学实验的的原理或操作方法不正确的是
| A.用溴水除去CO2中混有的SO2 |
| B.配制硫酸亚铁溶液时,要加入少量还原铁粉 |
| C.用固体NaOH与NH4Cl混和,在玻璃试管中加热制NH3 |
| D.用Fe3+检验工业废水中是否含有苯酚 |
甲、乙两容器都发生反应2 A(g)+B(g) 3C(g),两容器温度和初始压强都相同。在甲恒容容器中充入2 mol A和1 mol B,达平衡后,C在平衡混合气中的体积分数为φ1、物质的量为n1;在乙恒压容器中充入1.4 mol A、0.7 mol B和0.6 mol C,达平衡后C在平衡混合气中的体积分数为φ2、物质的量为n2。下列说法中正确的是()
3C(g),两容器温度和初始压强都相同。在甲恒容容器中充入2 mol A和1 mol B,达平衡后,C在平衡混合气中的体积分数为φ1、物质的量为n1;在乙恒压容器中充入1.4 mol A、0.7 mol B和0.6 mol C,达平衡后C在平衡混合气中的体积分数为φ2、物质的量为n2。下列说法中正确的是()
A.φ1>φ2 B.n1>n2C.n1=n2 D.φ1<φ2
在由水电离出的c(H+)=1×10-12 mol·L-1的溶液中,一定能大量共存的离子组是( )
A.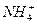 、Ba2+、 、Ba2+、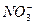 、Cl- 、Cl- |
B.Cl-、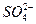 、Na+、K+ 、Na+、K+ |
C.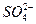 、 、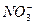 、Fe2+、Mg2+ 、Fe2+、Mg2+ |
D.Na+、K+、ClO-、I- |
X、Y、Z、W原子系数依次增加的短周期元素。已知①X、Y的氢化物的熔沸点在所在族中是最高,且常温下X、Y的氢化物的状态不同。②Y与Z是同一族。下列说法正确的是()
| A.四种元素中,原子半径最大的是W |
| B.X元素的最高价氧化物对应的水化物酸性最强 |
| C.单质的氧化性:W > Z |
| D.气态氢化物的熔点和沸点:Z> Y |