用过量的H2SO4、NaOH、NH3·H2O、NaCl等溶液,按下列步骤分离五种离子,则溶液①、②、③、④是 ( )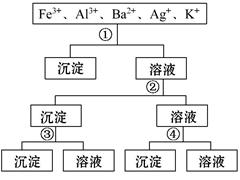
| A.①NaCl ②NaOH ③NH3·H2O ④H2SO4 |
| B.①H2SO4 ②NaOH ③NH3·H2O ④NaCl |
| C.①H2SO4 ②NH3·H2O ③NaOH ④NaCl |
| D.①NaCl ②NH3·H2O ③NaOH ④H2SO4 |
将Fe、Cu、Fe2+、Fe3+和Cu2+盛于同一容器中充分反应,如Fe有剩余,则容器中只能有()
| A.Cu、Fe3+ | B.Fe2+、Fe3+ |
| C.Cu、Cu2+、Fe | D.Cu、Fe2+、Fe |
下列离子的检验方法合理的是( )
| A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+ |
| B.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+ |
| C.向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+ |
| D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有Fe2+, 不含有Mg2+ |
下列四个反应可用H++OH-=H2O这个离子方程式表示的是()
| A.Ba(OH)2溶液与稀硫酸 |
| B.Cu(OH)2与稀硫酸 |
| C.NaOH溶液与稀硫酸 |
| D.NH3•H2O与稀硫酸 |
下列物质属于电解质的是 ()
①NaOH ②BaSO4③Cu ④蔗糖⑤CO2
| A.①② | B.①②⑤ |
| C.③④ | D.①⑤ |
在无色透明的强酸性溶液中,能大量共存的是( )
A.Na+、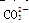 、Ca2+、 、Ca2+、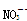 |
B.Na+、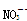 、Al3+、Cl 、Al3+、Cl |
C.K+、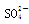 、Cl-、Cu2+ 、Cl-、Cu2+ |
D.Ba2+、Cl-、K+、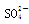 |