已知:
①NaHSO3====Na++H++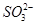 ;
;
②NaHSO4====Na++H++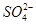 ;
;
③H2SO4====2H++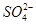 ;
;
④Ca(OH)2====Ca2++(OH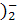
上述物质在水溶液中的电离方程式书写错误的是 ( )
| A.①② | B.① | C.③④ | D.①④ |
下列对应的表达方式错误的是
A.Cl-的结构示意图 |
B.2—甲基丁烷 |
C.碳-12原子 C C |
D.硫离子的核外电子排布式 1s22s22p63s23p4 |
环境问题与我们的生活息息相关,也是目前召开的两会热点之一,家用合成洗衣粉的主要成份是对十二烷基苯磺酸钠,为提高洗衣粉的洗涤效果,往往加入一定量的下列助洗剂,其中对环境有较严重影响的是
| A.磷酸钠(Na3PO4) | B.硫酸钠(Na2SO4) |
| C.硅酸钠(Na2SiO3) | D.碳酸钠(Na2CO3) |
已知X、Y、Z、L四种元素是组成蛋白质的基础元素且原子序数依次增大。回答下列问题:
(1)L的元素符号为________ ;Y元素原子核外电子中,未成对电子数与成对电子数之比为______;四种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。
(2)Z、X两元素按原子数目比l∶3可构成分子A,A的电子式为________;B分子也由Z、X两元素组成,作为运送飞船的火箭燃料,常温下是一种液态化合物。已知该化合物的相对分子质量为32,其中X元素的质量分数为12.5 %,且该分子结构中只有单键。则B的结构式为____________。若64 g B分子与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,还放出3000 kJ的热量,写出该反应的热化学方程式。
(3)硒(Se)是人体必需的微量元素,与元素L同一主族,该族第2 ~5周期元素单质分别与H2反应生成l mol气态氢化物产生的热量数据如下,其中能表示生成1 mol硒化氢所产生的热量的是__________(选填字母编号)。
a.—99.7 kJ b.—29.7 kJ c.+20.6 kJ d.+241.8 kJ
已知硫铁矿在沸腾炉中煅烧,通入沸腾炉中的气体原料是空气,其中N2的体积分数为0.80,则沸腾炉排出的气体中SO2的体积分数可能是
| A.0.13 | B.0.15 | C.0.22 | D.0.26 |
向1.00 L 0.3mol / L的NaOH溶液中缓慢通入0.2 mol CO2气体,使其完全反应,对反应后的溶液,下列判断正确的是
| A.c(OH-) > c(HCO3-) |
| B.c(HCO3-) > c(CO32-) |
| C.c(Na+) = 2c(CO32-) + 2c(HCO3-) + 2c(H2CO3) |
| D.c(Na+)+c(H+) = c(HCO3-)+2c(CO32-)+c(OH-) |