“PM2.5”是指大气中直径小于或等于2.5微米的颗粒物,它与空气中的SO2接触时,SO2会部分转化为SO3。则“PM2.5”的颗粒物在酸雨形成过程中主要的作用是下列的 ( )
| A.还原作用 | B.氧化作用 |
| C.催化作用 | D.抑制作用 |
下列根据实验操作和现象所得出的结论不正确的是
| 实验操作 |
实验现象 |
结论 |
|
| A |
向硅酸钠溶液中滴加1滴酚酞,再逐滴加入稀盐酸至红色褪去 |
试管里出现凝胶 |
酸性:盐酸>硅酸 |
| B |
在酒精灯上加热铝箔 |
铝箔熔化但不滴落 |
熔点:氧化铝>铝 |
| C |
向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液 |
有白色沉淀生成 |
该溶液中一定含有SO42- |
| D |
向某无色溶液中先滴加氯水,再加少量CCl4,振荡,静置 |
溶液分层,下层为橙红色 |
溶液中含有Br- |
将足量的CO2不断通入NaOH、Ba(OH)2、NaAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为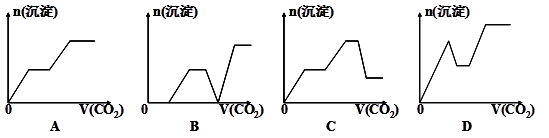
有Mg、Al、Fe、Cu四种金属,若两两混合,取混合物26 g与足量稀硫酸反应产生标准状况下氢气11.2 L,则此混合物的可能组合最多有
| A.2种 | B.3种 | C.4种 | D.5种 |
R2O8n-在一定条件下可以把Mn2+氧化成MnO4-,若反应中R2O8n-变为RO42-,又知反应中氧化剂与还原剂的物质的量之比为5∶2,则n值为
| A.1 | B.2 | C.3 | D.4 |
下列说法或做法正确的是
| A.硅是地壳中含量位居第二的元素,玛瑙、光导纤维的主要成分为SiO2 |
| B.金属钠着火燃烧时,用泡沫灭火器灭火 |
| C.铝比铁活泼,所以铝比铁更容易被腐蚀 |
| D.赏心悦目的雕花玻璃是用烧碱对玻璃进行刻蚀而制成的 |