Na2O2、Cl2、SO2等均能使品红溶液褪色,下列说法正确的是 ( )
| A.Na2O2、Cl2、SO2依次属于电解质、单质、非电解质 |
| B.标准状况下,1 mol Na2O2和22.4 L SO2反应生成Na2SO4,转移电子数目为NA |
| C.等物质的量Cl2和SO2同时通入品红溶液,褪色更快 |
| D.在Na2O2中阴阳离子所含的电子数目相等 |
下列反应的离子方程式正确的是
| A.氯化铝溶液中滴入氨水:Al3++3OH-→ Al(OH)3↓ |
| B.硫酸铁溶液中通入硫化氢气体:2Fe3++3H2S → 2FeS↓+ S↓+ 6H+ |
C.苯酚钠溶液中通入二氧化碳气体: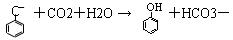 |
| D.NaHSO4溶液中滴入足量的Ba(OH)2溶液: |
H++SO42-+Ba2++OH-→ BaSO4↓+H2O
除去下列物质中少量杂质的方法正确的是
| A.除去CO2中混有的HCl:用饱和碳酸钠溶液洗气 |
| B.除去NO2中混有的NO:用水洗气 |
| C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如图,则原混合溶液中MgCl2与FeCl3的物质的量之比为
A.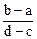 |
B.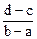 |
C.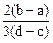 |
D.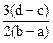 |
在标准状况下,将NO、NO2、O2三种气体按一定比例充满一固定容积的容器,并将该容器倒置在水槽中,充分反应后,容器中无气体剩余,所得溶液的浓度为Mmol/L。则M的取值范围是
| A.0<M<1/22.4 | B.1/39.2<M<1/22.4 |
| C.1/28<M<1/22.4 | D.1/39.2<M<1/28 |
下述实验不能达到预 期目的的是
期目的的是
| 编号 |
实验内容 |
实验目的 |
| A |
将SO2通入酸性KMnO4溶液中 |
证明SO2具有漂白性 |
| B |
将Cl2通入NaBr溶液中,然后加入CCl4,振荡、静置 |
比较氯与溴的氧化性强弱 |
| C |
将铜片分别与浓、稀硝酸反应 |
探究浓、稀硝酸氧化性的相对强弱 |
| D |
向盛有20g蔗糖的烧杯中加入几滴水,搅拌均匀。再加入少许浓硫酸,迅速搅拌。 |
探究浓硫酸的脱水性 |