下图是关于反应A2(g)+3B2(g)  2C(g)(正反应为放热反应)的平衡移动图形,影响平衡移动的原因是
2C(g)(正反应为放热反应)的平衡移动图形,影响平衡移动的原因是
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时使用适宜的催化剂 |
| D.增大反应物浓度,同时减小生成物浓度 |
某结晶水合物的化学式为R•nH2O,其相对分子质量为M。25℃时,将a g该晶体溶于b g H2O中恰好形成V mL饱和溶液。下列表达式正确的是
A.饱和溶液物质的量浓度为: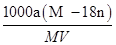 1000 a(M -18n) mol/L 1000 a(M -18n) mol/L |
B.饱和溶液溶质的质量分数为: |
C.25℃时R的溶解度为: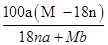 g/100 g H2O g/100 g H2O |
D.饱和溶液的密度为: g/mL g/mL |
常温下,取0.3 mol/L HY溶液与0.3 mol/L NaOH溶液等体积混合(不计混合后溶液体积变化),测得混合溶液的pH=9,则下列说法(或关系式)正确的是
| A.混合溶液中由水电离出来的c(OH-)=1×10-9 mol/L |
| B.混合溶液中离子浓度大小次序为:c(Y-)>c(Na+)>c(OH-)>c(H+) |
| C.c(OH-)=c(HY)=c(H+)=1×10-9 mol/L |
| D.c(Na+)=c(Y-)+c(HY)="0.3" mol/L |
今有一混合物的水溶液,只可能肯有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀生成;
(2)第二份加足量NaOH溶液后,收集到气体0.05mol;
(3)第三份加足量BaCl2溶液后,得干燥沉淀4.3g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,以下推测正确的是
| A.K+可能存在 | B.混合溶液中c(CO32-)为1 mol/L |
| C.Cl-一定存在 | D.Ba2+一定不存在,Mg2+可能存在 |
下列反应的离子方程式错误的是
| A.等物质的量的Ba (OH)2与NH4HSO4在溶液中反应: Ba2++2OH-+NH4++H++SO42-  BaSO4+NH3•H2O+H2O BaSO4+NH3•H2O+H2O |
B.氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3+3H+ Fe3++3H2O Fe3++3H2O |
C.足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-+H2O 2HCO3- 2HCO3- |
D.酸性条件下KIO3溶液和KI溶液反应生成I2:IO3-+5I-+3H2O  3I2+6OH- 3I2+6OH- |
一定量的锌粒与足量稀硫酸反应,向反应混合液中加入某些物质,下列判断正确的是
| A.加入少量水,产生H速率减小,H2体积不变 |
| B.加入NH4HSO4固体,产生H2速率不变,H2体积不变 |
| C.加入CH3COONa固体,产生H2速率减小,H2体积减小 |
| D.滴加少量CuSO4溶液,产生H2速率变大,H2体积减小 |