分类法在化学学科发展中起到了非常重要的作用,下列分类依据合理的是
①根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物和两性氧化物等
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否有丁达尔现象分为溶液、胶体和浊液
④根据组成元素的种类将纯净物分为单质和化合物
⑤根据电解质的水溶液导电能力的强弱将电解质分为强电解质和弱电解质
| A.②④ | B.②③④ | C.①③⑤ | D.①②④ |
下列八种物质:①甲烷、②苯、③聚乙烯、④聚异戊二烯、⑤2-丁炔、⑥环已烷、⑦邻二甲苯、⑧环已烯,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是
| A.③④⑤⑧ | B.④⑤⑦⑧ | C.④⑤⑧ | D.③④⑤⑦⑧ |
可用于鉴别以下三种化合物最合理的一组试剂是 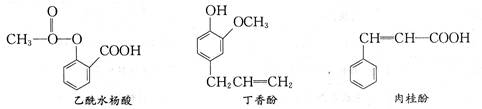
①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④氢氧化钠溶液
| A.②与③ | B.③与④ | C.①与④ | D.①与② |
已知乙烯醇不稳定,可自动转化成乙醛:CH2=CH-OH→CH3CHO.乙二醇在一定条件下发生脱水反应(有消去、有羟基和羟基之间反应形成“C—O—C”结构),所得产物的结构简式有人写出下列几种: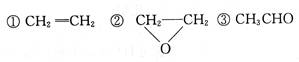
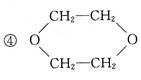
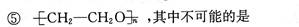
| A.只有① | B.②③ | C.③④ | D.④⑤ |
下列对有机物结构或性质的描述,错误的是
| A.一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 |
| B.光照下2,2—二甲基丙烷与Br2反应其一溴取代物只有一种 |
| C.甲苯与浓硫酸、浓硝酸的混合酸在30℃时主要生成邻硝基甲苯和对硝基甲苯 |
| D.苯酚钠溶液中通入少量CO2生成苯酚,同时生成碳酸钠 |
某烃1 mol最多能和2 mol HCl加成,生成氯代烃,此氯代烃l mol能和6 mol Cl2发生取代反应,生成物中只有碳氯两种元素,此烃为
| A.C2H2 | B.C2H4 | C.C3H4 | D.C6H6 |