下列有关溶液组成的描述合理的是
| A.由水电离出的c(H+)=10-13mol/L的溶液中可能存在:HCO3-、K+、Na+、Cl- |
B.酸性溶液中可能大量存在Na+、ClO 、SO42-、I 、SO42-、I |
| C.含有0.1 mol/L Fe3+ 的溶液中可以大量存在:K+、Mg2+、I-、NO3- |
| D.室温下,pH=l的溶液中一定可以存在:Na+、Fe3+、NO3-、SO42- |
某稀硫酸和稀硝酸的混合溶液200ml,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解m g。向另一份中逐渐加入铁粉,产生的气体量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)下列分析或结果错误的是()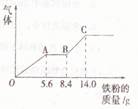
| A.第二份溶液中最终溶质为FeSO4 |
| B.原混合酸中NO3-物质的量为0.1mol |
| C.m值为9.6 |
| D.H2SO4浓度为2.5mol/L |
在15.2g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4g沉淀,则下列表示气体X组成的选项中合理的是()
| A.0.3mol NO、0.1mol NO2 | B.0.3mol NO2 |
| C.0.6mol NO | D.0.3mol NO2、0.1mol NO |
下列实验过程中,始终无明显现象的是()
| A.NO2通入FeSO4溶液中 |
| B.CO2通入CaCl2溶液中 |
| C.NH3通入AgNO3溶液中 |
| D.SO2通入Ba(NO3)2 |
在一定条件下发生下列反应,少量的物质可以反应完的是()
| A.过量的MnO2和少量的浓HCl | B.过量的铜和少量的浓硫酸溶液 |
| C.过量的氮气和少量的氢气合成氨 | D.过量的铁和少量的硝酸 |
下列溶液中微粒的物质的量浓度关系正确的是()
| A.在0.1mol/L NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-) |
| B.在0.1mol/L Na2CO3溶液中:2c(Na+)= c(HCO3-)+c(CO32-)+ c(H2CO3) |
| C.物质的量浓度相等的CH3COOK和CH3COOH溶液中,溶液显酸性:c(CH3COO-)>c(CH3COOH) |
| D.物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中的c(NH4+):①>②>③ |