下列实验操作与预期实验目的或所得实验结论一致的是
| 选项 |
实验操作 |
实验目的或结论 |
| A |
向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤 |
除去MgCl2溶液中少量FeCl3 |
| B |
向某溶液中加入BaCl2溶液生成白色沉淀,继续加稀硝酸沉淀不消失 |
证明溶液中含有SO42- |
| C |
向某溶液中加入稀盐酸,放出无色无味气体,将气体通入澄清石灰水 ,石灰水变浑浊 |
证明该溶液中存在CO32- |
| D |
向0.1mol•L-1FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色 |
说明Fe2+具有氧化性 |
工业上将苯的蒸气通过赤热的铁合成一种可作传热载体的化合物,该化合物分子中苯环上的一氯代物有3种,1mol该化合物催化加氢时最多消耗6mol氢气,判断这种化合物可能是
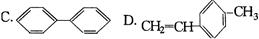
将 转变为
转变为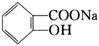 的方法是
的方法是
| A.与足量NaOH溶液共热,再通入足量CO2气体 |
| B.与稀硫酸共热后,再加入足量NaOH溶液 |
| C.加热该物质的溶液,再通入足量的Na |
| D.与稀硫酸共热后,加入足量的Na2CO3溶液 |
如图表示4—溴环己烯所发生的4个不同反应。其中,产物只含有一种官能团的反应是
| A.①④ | B.③④ | C.②③ | D.①② |
下列除杂质(括号内为杂质)的方法正确的是
| A.苯(甲苯):加酸性KMnO4溶液,振荡后分液 |
| B.甲烷(乙烯):通过盛有溴水的洗气瓶 |
| C.乙醇(丙三醇):用分液漏斗分液 |
| D.苯(苯酚):加浓溴水,后过滤 |
由—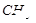 、—OH、
、—OH、 、—COOH四种基团两两组合而成的有机物中,其水溶液能使石蕊变红的有
、—COOH四种基团两两组合而成的有机物中,其水溶液能使石蕊变红的有
| A.5种 | B.4种 | C.3种 | D.2种 |