(11分)A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周期;E元素原子的最外层电子数比次外层电子数少2;A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物。请回答:
(1)C离子的原子结构示意图_______________;D在周期表的位置___________________。
(2)C和E两种元素相比较,原子得电子能力较强的是(填元素名称)________________,以下三种说法中,可以验证该结论的是(填写编号)______________;
a.比较这两种元素的常见单质的沸点
b.二者形成的化合物中,C元素的原子显负价
c.比较这两种元素气态氢化物的稳定性
(3)A、B、C、E可形成两种酸式盐(均含有该四种元素),它们都含有的化学键类型是_________,这两种酸式盐在水溶液中相互反应的离子方程式为_______________________________。
(4)C与D形成的某种化合物可作潜水面具中的供氧剂,每生成标准状况下11.2LO2,转移的电子数是___。
写出下列叙述中有关物质的结构简式:
⑴分子式为C3H7Br的卤代烃经消去反应后得到的有机物是__________________;
⑵能与金属钠反应,但不能与氢氧化钠反应的芳香族化合物C7H8O是____________;
⑶含C、H、O三种元素的有机物,燃烧时消耗的氧气和生成的CO2、H2O之间物质的量之比为1︰2︰2,则此类有机物中最简单的一种是________________。
在下列几种有机物中(用编号填写)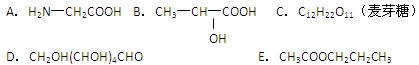
⑴既能发生银镜反应,又能发生水解反应的是。
⑵既能与酸反应,又能与碱反应的是。
⑶既能发生酯化反应,又能发生消去反应的是。
⑷酸性条件下水解产物是两种相对分子质量相等的有机物是。
(12)某元素R原子的核外电子数等于核内中子数,该元素的单质2.8g与氧气充分反应,生成6.0g的化合物RO2。请回答:
(1)元素R的原子序数是。
(2)元素R的原子共有个电子层,能量最低的电子层中共有个电子。
(3)写出元素R的最高价氧化物对应水化物的化学式,它的酸性比碳酸的酸性。
已知X、Y、Z、W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z、W四种元素的符号:
X、Y 、Z、W
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为,。
(3)由X、Y、Z所形成的离子化合物是,它与W的最高氧化物的水化物的浓溶液加热时反应的离子方程式是。
(1)写出电子式:
KCl;CO2
(2)用电子式表示下列化合物的形成过程:
CaF2:
NH3: