下列有关说法正确的是 ( )
| A.1 mol Cl2参加反应转移电子数一定为2NA |
B.反应Li2NH+H2 LiNH2+LiH中H2既是氧化剂又是还原剂 LiNH2+LiH中H2既是氧化剂又是还原剂 |
| C.在反应KIO3+6HI===KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA |
D.根据反应中HNO3(稀)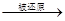 NO,而浓硝酸 NO,而浓硝酸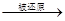 NO2可知,氧化性HNO3(稀)>浓硝酸 NO2可知,氧化性HNO3(稀)>浓硝酸 |
在一密闭容器中进行如下反应:2SO2(气)+O2(气) 2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
| A.SO2为0.4mol/L、O2为0.2mol/L | B.SO2为0.25mol/L |
C.SO2 、SO3均为0.15mol/L 、SO3均为0.15mol/L |
D.SO3为0.4mo l/L l/L |
某学生的实验报告所列出的下列数据中合理的是
| A.用10mL量筒量取7.13mL稀盐酸 |
| B.用托盘天平称量25.20g NaCl |
| C.用广泛pH试纸测得某溶液的pH为2.3 |
| D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL |
现有含Fe(NO3)3、Cu(NO3)2、HNO3的某稀溶液,若向其中逐步加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示,则该溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为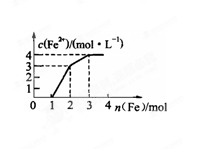
| A.1∶1∶1 | B.1∶3∶1 | C.3∶3∶8 | D.1∶1∶4 |
NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.7.8 g Na2S和7.8 g Na2O2中含有的阴离子数目均为0.1 NA |
| B.0.1mol·L-1的NaHSO4溶液中含有阳离子的物质的量为0.2mol |
| C.常温常压下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24 L |
| D.l.8 g188O2分子与1.8 g188O3分子中含有的中子数不相同 |
已知短周期元素的离子aW2+、b X+ 、cY2-、d Z- 具有相同的电子层结构,下列正确的是
、cY2-、d Z- 具有相同的电子层结构,下列正确的是
| A.原子序数:a > b > c > d | B.离子的还原性:Y 2- > Z-、 2- > Z-、 |
| C.氢化物的稳定性H2Y > HZ | D.原子半径X < W |