将两种硫酸盐按一定比例混合后共熔,可制得化合物X,X溶于水能电离出K+、Cr3+、SO42-,若将2.83 g X中的Cr3+全部氧化为Cr2O72-后,溶液中的Cr2O72-可和过量KI溶液反应,得到3.81 g I2,反应的离子方程式为:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,若向溶有2.83 g X的溶液中,加入过量的BaCl2溶液,可得到4.66 g白色沉淀。由此可推断出X的化学式为
| A.K2SO4·2Cr2(SO4)3 | B.2K2SO4·Cr2(SO4)3 | C.K2SO4·1/2Cr2(SO4)3 | D.K2SO4·Cr2(SO4)3 |
用来表示可逆反应:2A(g)+B(g)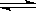 3C(g)(正反应放热)的正确图象是下图中的
3C(g)(正反应放热)的正确图象是下图中的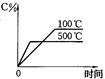

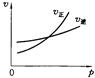

A B C D
在一混合溶液中含有KCl、KBr、K2CrO4,其浓度均为0.01 mol·L-1,向溶液中逐滴加入0.01 mol·L-1AgNO3溶液时,最先和最后沉淀的物质是(AgCl、 AgBr、 Ag2CrO4的Ksp分别为1.77×10-10、5.35×10-13、1.12×10-12)
| A.AgBr、AgCl | B.Ag2CrO4、AgCl |
| C.AgBr、Ag2CrO4 | D.同时沉淀 |
体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2 + O2 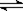 2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为
| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
有甲、乙两醋酸稀溶液,测得甲的pH=2,乙的pH=3,下列推断中正确的是
| A.物质的量浓度c(甲)=c(乙) |
| B.甲中由水电离产生的H+的物质的量浓度是乙的0.1倍 |
| C.中和等物质的量浓度等体积的NaOH溶液需甲、乙两酸的体积V(乙)=10V(甲) |
| D.甲中的c(OH-)为乙中c(OH-)的10倍 |
下列说法正确的是
| A.电离平衡常数受溶液浓度的影响 |
| B.电离平衡常数可以表示弱电解质的相对强弱 |
| C.电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大 |
| D.H2CO3的电离常数表达式:K= |