有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂溶解在亚硫酰氯(SOCl2)中形成,电池的总反应式为8Li+3SOCl2=6LiCl+Li2SO3+2S,则下列叙述正确的是 ( )
| A.用该电池电解CuCl2溶液产生2.24LCl2时,有0.2mol电子转移 |
| B.金属锂作电池的负极,石墨作电池的正极,加入硫酸可提高电解质的导电性 |
| C.电池工作(放电)过程中,SOCl2被还原为Li2SO3 |
| D.电池工作过程中,负极消耗的锂与正极生成的硫质量之比为7:8 |
某一有机物A可发生下列变化:
已知c为羧酸,且.C、E均不能发生银镜反应,则A的可能结构有
A.1种 B.4种 C.3种 D.2种
某有机物A是农药生产中的一种中间体,其结构简式如图所示。下列叙述中正确的是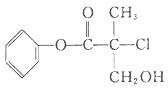
| A.有机物A属于芳香烃 |
| B.有机物A可以与Br2的CCl4溶液发生加成反应 |
| C.有机物A与浓硫酸混合加热,可以发生消去反应 |
| D.1 molA与足量的NaOH溶液反应,最多可以消耗3 mol NaOH |
NA为阿伏加德罗常数的值,下列有关叙述不正确的是
A.0.1 mol C3H6Cl2中化学键总数为 |
B.42 g乙烯中含碳原子数为3  |
C.标准状况下,1L苯完全燃烧生成的气态产物的分子数为(6/22. 4) |
D.0.1 mol乙醇完全燃烧所消耗的氧分子数一定为0.3  |
下列各组有机物中,无论以何种比例混合,只要二者的物质的量之和不变,完全燃烧时消耗的氧气及生成的水的物质的量也不变的是
按下列路线制聚氯乙烯,没有发生的反应类型是
| A.加成反应 | B.消去反应 | C.取代反应 | D.加聚反应 |