化学方程式可简明地体现元素及其化合物的性质。已知:氧化还原反应:
2FeCl3 + 2HI = 2FeCl2 + I2 + 2HCl; 2Co(OH)3 + 6HCl = 2CoCl2 + Cl2↑ + 6H2O
2Fe(OH)2 + I2 + 2KOH= 2Fe(OH)3 + 2KI; 3I2 + 6KOH=" 5KI" + KIO3 + 3H2O
复分解反应:
2HSCN + K2CO3 =" 2KSCN" + CO2 ↑ + H2O; KCN + CO2 + H2O =" HCN" + KHCO3
热分解反应:4NaClO  3NaCl + NaClO4;NaClO4
3NaCl + NaClO4;NaClO4 NaCl + 2O2↑
NaCl + 2O2↑
下列说法正确是( )
| A.氧化性(酸性溶液):FeCl3 > Co(OH)3> I2 | B.还原性(碱性溶液):Fe(OH)2 > I2 > KIO3 |
| C.热稳定性:NaCl > NaClO > NaClO4 | D.酸性(水溶液):H2CO3 > HSCN > HCN |
下列离子方程式正确的是()
| A.乙酸与碳酸钠溶液反应:2H++CO32-== CO2↑+H2O |
| B.澄清石灰水中加入过量的碳酸氢钠溶液:Ca2+ + HCO + OH-= CaCO3↓ + H2O |
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O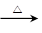 2C6H5OH+CO32- 2C6H5OH+CO32- |
D.甲醛溶液与足量的银氨溶液共热HCHO+4[Ag(NH3)2]++4OH- CO32-+2NH4++ 4Ag↓+ 6NH3↑+ 2H2O 。 CO32-+2NH4++ 4Ag↓+ 6NH3↑+ 2H2O 。 |
有一种解热镇痛药的结构简式是: ,当这种物质完全水解时,能够产生的产物有()
,当这种物质完全水解时,能够产生的产物有()
| A.2种 | B.3种 | C.4种 | D.5种 |
某有机物结构简式为 ,该有机物不可能发生的反应( )
,该有机物不可能发生的反应( )
①氧化②取代③加成④消去⑤还原⑥酯化⑦水解⑧加聚
| A.② | B.④ | C.⑥ | D.⑧ |
下列有关有机物的说法错误的是()
| A.酸性KMnO4溶液既可以用于鉴别CH4与CH2=CH2,但不用于除去CH4中混有的CH2=CH2 |
| B.乙醇、乙酸和乙酸乙酯均能发生取代反应 |
| C.苯、甲苯互为同系物,都能发生氧化反应和加成反应 |
| D.在苯酚溶液中,滴入少量稀溴水,立即产生白色沉淀 |
下列有关实验及操作的叙述中,错误的是( )
| A.用水将苯、乙酸、四氯化碳区分开来 |
| B.在实验室中通常将钠保存在四氯化碳里 |
| C.用稀硝酸洗去残留在试管壁上的银 |
| D.如果苯酚溶液沾到皮肤上,应立即用酒精洗涤 |