下列各组离子能大量共存,向溶液中通入足量相应气体后,各离子还能大量存在的是
| A.氯气:K+ Ba2+ SiO32- NO3- | B.二氧化硫:Na+ NH4+ SO32- C1- |
| C.氨气:K+ Na+ AlO2-.CO32- | D.甲醛:Ca2+ Mg2+ MnO4- NO3- |
已知热化学方程式:SO2(g)+ 1/2O2(g)  SO3(g) △H= ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为()
SO3(g) △H= ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为()
| A.196.64kJ | B.196.64kJ/mol | C.<196.64kJ | D.>196.64kJ |
 图中表示外界条件(t、p)的变化对下列可逆反应的影响:
图中表示外界条件(t、p)的变化对下列可逆反应的影响:
L(s)+G(g)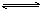 2R(g);△H>0,y 轴表示的是 ( )
2R(g);△H>0,y 轴表示的是 ( )
| A.平衡时,混合气中G的百分含量 | B.G的转化率 |
| C.平衡时,混合气中R的百分含量 | D.L的转化率 |
甲乙两容器中发生相同的反应: A(g) + 3B(g) 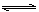 2C(g) ,甲恒容、乙恒压,温度相同而恒定。起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02molC,开始时两容器压强相等,最后分别达到平衡。下列有关它们平衡状态的叙述正确的是( )
2C(g) ,甲恒容、乙恒压,温度相同而恒定。起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02molC,开始时两容器压强相等,最后分别达到平衡。下列有关它们平衡状态的叙述正确的是( )
A.体积:甲可能小于乙 B.C的物质的量:甲一定小于乙
C.压强:甲可能大于乙 D.A、C浓度比值c(A)/c(C):甲一定小于乙
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是()
| A.CH3OH(l)+3/2O2(g) |
| B.2CH3OH(l)+3O2(g) |
| C.2CH3OH(l)+3O2(g) |
| D.2CH3OH(l)+3O2(g) |
在一定温度下,反应A2(g)+B2(g) 2AB(g)达到平衡状态的标志是( )
2AB(g)达到平衡状态的标志是( )
| A.单位时间内生成n molA2,同时生成n molAB |
| B.容器内混合气体的平均相对分子质量不随时间变化 |
| C.单位时间内生成2n molAB,同时生成n molB2 |
| D.单位时间内一个A-A键断裂,同时生成二个A-B键 |