(实验班做)已知碳化铝(Al4C3)与水反应生成氢氧化铝和甲烷。为了探究甲烷性质,某同学设计如下两组实验方案;甲方案探究甲烷与氧化剂反应(如图1所示);乙方案探究甲烷与氯气反应的条件(如图2所示)。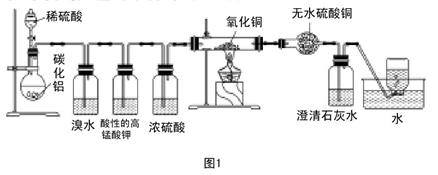
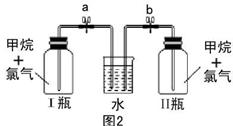
甲实验现象:溴水无颜色变化,澄清石灰水变浑浊,无水硫酸铜变蓝色。乙实验操作过程:通过排饱和食盐水的方法收集两瓶甲烷与氯气(体积比为1∶4)混合气体(I、II),II瓶用预先准备好的黑色纸套套上,I瓶放在光亮处(不要放在日光直射的地方,以免引起爆炸)。按图2安装好装置,并加紧弹簧夹a和b。
(1)写出碳化铝与硫酸反应的化学方程式 。
(2)实验甲中浓硫酸的作用是 ,集气瓶中收集到的气体能否直接排入空气中? (填“能”或“否”)。
(3)下列对实验甲有关现象与结论的叙述都正确的是( )
| A.酸性高锰酸钾溶液不褪色,结论是通常条件下,甲烷不能与强氧化剂反应 |
| B.硬质试管里黑色粉末无颜色变化,结论是甲烷不与氧化铜反应 |
| C.硬质试管里黑色粉末变红色,推断氧化铜与甲烷反应只生成水和二氧化碳 |
| D.甲烷不能与溴水反应,推知甲烷不能与卤素单质反应 |
(4)写出硬质试管里可能发生的化学方程式 ,(按甲烷与氧化铜物质的量之比4:7)
(5)过一段时间,打开图2的a、b弹簧夹,I、II中观察到现象是 。
利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如下。根据要求填空:
(1)B 装置有三种功能:①________________________________________;
②_______________________________________________________________;
③_______________________________________________________________。
(2) D 装置中的石棉上均匀附着KI粉末,其作用是__________________________。
(3)E装置中除了有盐酸生成外,还含有有机物,从 E 中分离出盐酸的最佳方法为
_________________。
(4)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内璧有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式_______________________________________。
(5)该装置还有缺陷,没有进行尾气处理,其尾气的主要成分是(填编号)_______。
| A.CH4 | B.CH3Cl |
C.CH2Cl2 | D.CHCl3 E.CCl4 |
(8分) 下图是实验室制备乙酸乙酯的实验装置。试回答:
(1)试管甲中加入的试剂顺序是()
A.乙醇、浓硫酸、乙酸
B.浓硫酸、乙醇、乙酸
C.浓硫酸、乙酸、乙醇
(2)甲处的试管内发生反应的化学方程式为:
(3)小试管乙中饱和Na2CO3的作用是( )
A、吸收乙醇
B、中和乙酸
C、增大溶液密度,降低乙酸乙酯在里面的溶解度
(4)乙装置中的导管未插入溶液的目的是。
(8分) 从右边选项中选择适当的试剂除杂,把相应的字母填写在表格内。
| 物质(括号内为杂质) |
答案 |
除杂试剂 |
||||
| (1) CO2气体(SO2) |
|
|||||
| (2) CH4气体(CH2=CH2) |
||||||
| (3) Na2CO3固体(NaHCO3) |
||||||
| (4) FeCl2溶液(FeCl3) |
我国规定:室内甲醛含量不得超过0.0 8mg·m-3。某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛(HCHO)的含量。
【查阅资料】KMnO4 ( H+)溶液为强氧化剂,可氧化甲醛和草酸。
4MnO4―+5HCHO+H+=4Mn2++5CO2↑+11H2O
2MnO4―+5H2C2O4+6H+=2Mn2++10CO2 ↑+8H2O
【实验一】
按如图所示装置进行采样
(1)由图可知甲醛的物理性质为
(2)空气中甲醛采样吸收装置中用到的玻璃仪器为:玻璃导管、
(3)为了使通过吸收装置的甲醛尽可能被吸收液吸收,可采取的措施是:(只写出一种即可)。
设置空气采集器为恒定流量0.5 L/min,采集20min。
【实验二】
量取10.00 mL 的甲醛吸收液转移到锥形瓶中,量取12.00 mL 1.00×10-3 mol·L-1 KMnO4溶液于锥形瓶中,并滴入几滴稀H2SO4备用。
(4)用1.00×10-3 mol·L-1标准草酸溶液进行滴定,当
时,达到滴定终点。
(5)记录滴定所消耗的草酸溶液的体积。重复实验2次,消耗草酸溶液的体积分别为10.90 mL、10.02 mL、9.98 mL。计算该居室内空气中甲醛的浓度为mg·m-3。
(6)若滴定过程中,发现滴定管下端开始有气泡,滴定后气泡消失,则测定结果将
(填“偏大”、“无影响”、“偏小”)
【实验三】
环境监测站工作人员采样后,将5.00 mL 的甲醛吸收液注入比色瓶中,再向比色瓶中注入显色试剂0.5 mL,盖紧瓶塞,摇匀,静置显色。当室内环境温度不同时,记录显色时间见下表。
| 环境温度/℃ |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
| 显色时间/min |
45 |
30 |
15 |
13 |
10 |
7 |
5 |
(7)由该表可以得出的结论是
(8)请用化学反应原理解释
(15分)已知CaSO4受热分解,由于受热温度不同,气体成分也不同。气体成分可能为SO2、SO3和O2中的一种、二种或三种。某化学课外活动小组准备通过系列实验探究CaSO4分解生成的气体,进而确定CaSO4分解的化学方程式。
【提出猜想】
Ⅰ.所得气体的成分可能只含 SO3一种;
Ⅱ.所得气体的成分可能含有二种;(填分子式)
Ⅲ.所得气体的成分可能含有 SO2、SO3、O2三种。
【设计实验】
该化学课外活动小组准备通过测定D装置的增重以及量筒中水的体积,来探究CaSO4分解生成的气体成分,进而确定CaSO4分解的化学方程式。
【实验过程】
根据上述实验方案进行试验。已知实验结束时,CaSO4完全分解。
请结合以下实验现象和记录的实验数据进行分析:
(1)若实验结束时,G中量筒没有收集到水,则证明猜想正确。(填Ⅰ或Ⅱ或Ⅲ)
(2)若实验结束时,装置D的总质量增加,能否断定气体产物中一定含有SO2而不含SO3?请说明理由:。
(3)该实验设计中,容易给测 定带来较大误差的因素有。
定带来较大误差的因素有。
(写出一种即可)
(4)经改进后,有两组同学进行该实验,由于加热时的温度不同,实验测得数据也不同,
相关数据如下:
| 实验小组 |
称取CaSO4 的质量(g) |
装置D增加 的质量(g) |
量取气体体积的装置测量的气体体积 (折算成标准状况下气体的体积) (mL) |
| 一 |
4.08 |
2. 56 56 |
224 |
| 二 |
5.44 |
2.56 |
448 |
请通过计算,推断第二组同学得出的CaSO4分解的化学反应方程式:
第二组:。