下列有关判断、叙述正确的是( )
| A.质量分数为W的氨水其浓度为C1 mol/L,则质量分数为2W的氨水,其浓度大于2C1 mol/L |
| B.3.2克的甲烷与标准状况下8.96 L的水所含有的氢原子数相同 |
| C.铅蓄电池中放电时转移2NA个电子,则电池内消耗4 mol H2SO4 |
| D.等质量的SO2与SO3所含有的氧原子数之比为5:6 |
在一个不传热且容积固定的密闭反应器里,有可逆反应:mA(g) + nB(g) 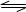 pC(g)+qD(g)当m、n、p、q为任意正整数时,该反应达到平衡的标志是( )
pC(g)+qD(g)当m、n、p、q为任意正整数时,该反应达到平衡的标志是( )
①体系的压强不再发生变化;
②体系的温度不再发生变化;
③各组分的物质的量浓度不再发生变化;
④各组分的质量分数不再发生变化;
⑤反应速率γA:γB: γC: γD = m:n:p:q;
⑥单位时间内,若消耗了m mol A物质,同时也消耗了qmolD物质
| A.①③⑤ | B.①④⑥ | C.②③④⑥ | D.③④⑤⑥ |
A、B、C、D四种气体之间可发生反应:aA + bB cC + d D,该反应在一定条件下建立平衡,改变条件,经足够长的时间后,体系发生了下列各种变化,其中能表明该平衡一定发生了转移的是( )
cC + d D,该反应在一定条件下建立平衡,改变条件,经足够长的时间后,体系发生了下列各种变化,其中能表明该平衡一定发生了转移的是( )
A.混合气的密度增大了
B.混合体系的压强增大了
C.正逆反应的速率相等,且都比原平衡状态的速率增大了
D.A气体在混合气中的含量升高了
一定条件下,通过下列反应可实现燃料烟气中硫的回收:SO2(g)+2CO(g)  2CO2(g)+S(l) ΔH <0下列说法正确的是( )
2CO2(g)+S(l) ΔH <0下列说法正确的是( )
| A.平衡前,随着反应的进行,容器内压强始终不变 |
| B.平衡时,其他条件不变,分离出硫,正反应速率加快 |
| C.平衡时,其他条件不变,升高温度可提高SO2的转化率 |
| D.其他条件不变,使用不同催化剂,该反应的平衡常数不变 |
下列不能用勒夏特列原理解释的事实是()
| A.棕红色的NO2加压后颜色先变深后变浅 |
| B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深 |
| C.黄绿色的氯水光照后颜色变浅 |
| D.合成氨工业使用高压以提高氨的产量 |
把3molP和2.5molQ置于2L密闭容器中发生如下反应:3P(g)+Q(g) xM(g)+2N(g)经5mim反应达平衡时,测知生成1molN,M的平均反应速率为0.1mol/(L.min),下列叙述错误的是
xM(g)+2N(g)经5mim反应达平衡时,测知生成1molN,M的平均反应速率为0.1mol/(L.min),下列叙述错误的是
| A.P的平均反应速率为0.15 mol/(L.min); |
| B.Q的转化率为25%; |
| C.Q的平衡浓度为1mol/L; |
| D.x的值是2。 |