如图装置中,容器甲内充入0.1 mol NO气体,干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体.恒温下,容器甲中活塞缓慢由D向左移动,当移至C处时容器体积缩小至最小,为原体积的9/ 10,随着CO2的继续通入,活塞又逐渐向右移动。(不考虑活塞的磨擦)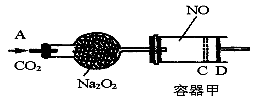
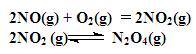
已知: 2Na2O2 + 2CO2= 2Na2CO3 + O2
(1)已知当活塞移至C处时,干燥管中物质的质量增加了2.24 g。
①此时,通入标准状况下的CO2气体 L ,容器甲中NO2转化为N2O4的转化率是
②活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至D处.则a值必 0.01(填大于、小于、等于),其理由是
(2)若改变干燥管中Na2O2的量,要通过调节甲容器的温度及通入的量CO2,使活塞发生从D到C,又从C到D的移动,则Na2O2的质量最小值应大于________g。
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应。能引发化学反应的碰撞称之为有效碰撞,这些分子称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位用kJ•mol-1表示。请认真观察下图,然后回答问题。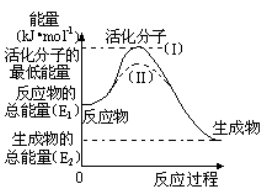
(1)图中反应是(填“吸热”或“放热”)反应,该反应(填“需要”或“不需要”)提供能量,该反应的△H=(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+1/2O2(g) ===H2O(g)△H=-241.8kJ•mol-1,该反应的活化能为167.2 kJ•mol-1,则其逆反应的活化能为。
(3)对于同一反应,图中虚线(II)与实线(I)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是。
在一定温度下,向AgI的饱和溶液中:(填“增大”、“减小”或“不变”)
(1)若加入AgNO3固体,c(I-)。
(2)若加入更多的AgI固体,则c(Ag+)。
(3)若加入固体AgBr,c(I-)。
有浓度为0.1 mol•L-1的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液中c(H+) 依次为a mol•L-1,b mol•L-1,c mol•L-1,其大小顺序为__________。
(2)等体积的以上三种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量依次为n 1mol,n2 mol,n3 mol,它们的大小关系为____________。
(3)中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为____________。
(4)与锌反应时产生氢(气)的速率分别为v1、v2、v3,其大小关系为____________
已知:2Al (s)+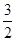 O2(g)===Al2O3(s)△H=" -1" 644.3 kJ• mol-1
O2(g)===Al2O3(s)△H=" -1" 644.3 kJ• mol-1
2Fe (s) +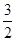 O2(g)===Fe2O3(s)△H=" -815.88" kJ• mol-1
O2(g)===Fe2O3(s)△H=" -815.88" kJ• mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式___________________________。
(11分) H是一种香料,可用下图的设计方案合成.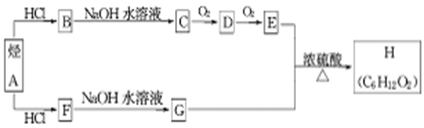
已知:①在一定条件下,有机物有下列转化关系: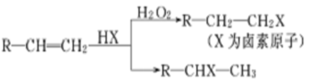
②烃A和等物质的量的HCl在不同的条件下发生加成反应,既可以生成只含有一个甲基的B,也可以生成含有两个甲基的F。
(1)D的结构简式为________________,其核磁共振氢谱有_____组峰。
(2)烃A→B的化学反应方程式是_______________________________。
(3)F→G的化学反应类型为__________。
(4)E+G→H的化学反应方程式_____________________________________。
(5)H有多种同分异构体,其中含有一个羧基,且其一氯代物有两种的是____________。(用结构简式表示)