为确定某溶液的离子组成,进行实验:
①测定溶液的pH值,溶液显碱性
②取少量溶液加稀盐酸至溶液呈酸性,产生能使澄清石灰水变浑浊的气体
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加Ag NO3溶液,产生白色沉淀。根据以上实验,以下对原溶液的推测正确的是
| A.一定有CO32-离子存在 | B.不能确定是否存在HCO3-离子存在 |
| C.一定有C1–离子存在 | D.一定有SO32-离子存在 |
食品添加剂关系到大家健康,下列物质中的添加剂作用不正确的是
| A |
B |
C |
D |
 |
 |
 |
 |
| 防治高血压 |
防治缺铁性贫血 |
做甜味剂 |
做防腐剂 |
如图装置中,在U形管底部盛有CCl4,分别在U形管两端小心倒入饱和食盐水和稀硫酸溶液,并使a、b两处液面相平,然后分别塞上插有生铁丝的塞子,密封好,放置一段时间后,下列有关叙述中错误的是
| A.铁丝在两处的腐蚀速率:a < b |
| B.a、b两处相同的电极反应式为Fe-2e-==Fe2+ |
| C.生铁丝中的碳在a、b两处分别作原电池的负极和正极 |
| D.一段时间后,a处液面高于b处液面 |
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,其负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是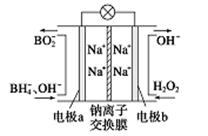
A.该电池的负极反应为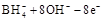  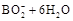 |
| B.电池放电时Na+从b极区移向a极区 |
| C.每消耗3 mol H2O2,转移的电子为3 mol |
| D.电极a采用MnO2作电极材料 |
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li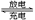 LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。下列有关LiFePO4电池说法正确的是
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。下列有关LiFePO4电池说法正确的是
| A.可加入硫酸以提高电解质的导电性 |
| B.放电时电池内部Li+向负极移动 |
| C.充电过程中,电池正极材料的质量不变 |
| D.放电时电池正极反应为:FePO4+Li++e-=LiFePO4 |
下列图示与对应的叙述相符的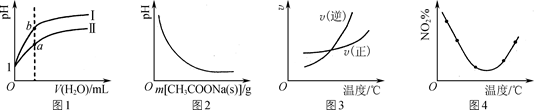
| A.图1表示相同温度下,相同体积、pH均为1的盐酸和醋酸溶液分别加水稀释时溶液pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.图2表示CH3COOH溶液中逐步加CH3COONa固体后,溶液pH的变化 |
| C.图3表示某可逆反应正、逆反应速率随温度变化,则该反应的正反应是吸热反应 |
| D.图4表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应: |
2NO2(g)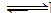 N2O4(g),相同时间后测得NO2体积分数的曲线,则该反应的正反应ΔH<0
N2O4(g),相同时间后测得NO2体积分数的曲线,则该反应的正反应ΔH<0