下列根据实验操作和现象所得出的结论正确的是
| |
实验操作 |
实验现象 |
结论 |
| A |
淀粉与稀H2SO4共热,再加银 氨溶液水浴加热 |
无银镜生成 |
淀粉水解产物无还原性 |
| B |
向某溶液中先滴加氯水,再滴 加少量KSCN溶液 |
溶液变成血红色 |
溶液中含有Fe2+ |
| C |
向NaAlO2溶液中滴加饱和NaHCO3溶液 |
有白色沉淀产生 |
验证两者都发生了水解反应,且相互促进 |
| D |
将CO2通入Na2SiO3溶液中 |
有白色沉淀生成 |
证明H2CO3酸性比H2SiO3强 |
下列物质与稀硫酸作用只得一种产物的是 ( )
| A.乙酸乙酯 |
| B.麦芽糖 |
| C.氯乙烷 |
| D.蔗糖 |
下列各对物质中,互为同系物的是 ( ) 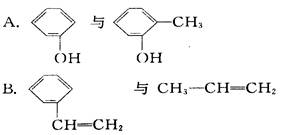
C. HCOOCH3与CH3COOH
D. C6H5OH与C5H5CH2OH
能够经过催化加氢得到2甲基戊烷的烯烃有 ( )
| A.2种 | B.3种 |
| C.4种 | D.5种 |
下列各有机物中,既能被高锰酸钾酸性溶液氧化,又能跟溴水发生取代反应的是 ( )
| A.苯乙烯 | B.苯酚水溶液 |
| C.苯甲醛 | D.甲醛水溶液 |
某有机物的氧化产物甲、还原产物乙都与钠反应放出H2,甲、乙在浓硫酸催化下反应生成丙,丙能发生银镜反应,这种有机物是 ( )
| A.甲酸 | B.甲醛 |
| C.甲醇 | D.甲酸甲酯 |