比较法是化学中研究物质性质的基本方法之一,请运用比较法解答下题。Na2O2几乎可与所有的常见气态非金属氧化物反应。如
2Na2O2+2CO2 ="=" 2Na2CO3+O2, Na2O2+CO = Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式: _________________;___________________。
(2)通过比较可知,当非金属元素处于____________价时,其氧化物与Na2O2反应有O2生成。
(3)依上述规律,写出Na2O2与N2O5反应的化学方程式________________________________。
实验室配制500ml 2mol·L-1的H2SO4溶液
(1)500ml 2mol·L-1的H2SO4溶液中所含溶质的质量是g。
(2)配制时,所需仪器应该有烧杯、玻璃棒、量筒、、。
(3)容量瓶在使用前,首先应检查。
(4)此实验中,玻璃棒的两个作用分别是、。
(5)下列操作会使配制的溶液浓度偏低的是(选填序号)
| A.没有将洗涤液转移到容量瓶 | B.定容时俯视刻度线 |
| C.容量瓶洗净后未干燥 | D.转移过程中有少量溶液测出 |
(12分)下图为苯和溴取代反应的改进实验装置。其中A为带支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑。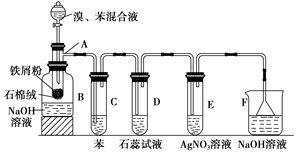
填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):_______________________________________。
(2)试管C中苯的作用是________________________________________________;
反应开始后,观察D试管,看到的现象为______________________________________。
(3)在上述整套装置中,具有防倒吸作用的仪器有_________________________(填字母)。
(4)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这三个优点外,还有一个优点是____________________________________________。
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯

(1)制备粗品
将12.5 mL环己醇加入试管A中,再加入l mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是____________,导管B除了导气外还具有的作用是_________。
②试管C置于冰水浴中的目的是______________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_______层(填上或下),分液后用_______ (填入编号)洗涤。
A.KMnO4溶液 B.稀H2SO4 C. Na2CO3溶液
②再将环己烯按下图装置蒸馏,冷却水从_________口进入,目的是__________________。
③收集产品时,控制的温度应在左右。以下区分环己烯精品和粗品的方法,合理的是_________。
A用酸性高锰酸钾溶液 B用金属钠 C测定沸点
已知Cl2+H2O  HCl+HClO。为了探究HClO的漂白性,某同学设计了如下的实验。
HCl+HClO。为了探究HClO的漂白性,某同学设计了如下的实验。
(1)通入Cl2后,从集气瓶A中干燥的红色布条没有褪色的现象可得出的结论是;
从集气瓶B中湿润的红色布条的现象可得出的结论是。
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是。
(1)实验室有下列仪器:
请从上述仪器中选择适当的仪器按要求填空。
(a)分离两种互不相溶的液体的仪器是__(填字母)。
(b)配制250ml0.1 mol·L-1的盐酸需要用到的仪器是_(填字母)。
(c)常用作配制一定物质的量浓度的仪器是_ _(填仪器名称)。
(d)若定容时加蒸馏水液面没到刻度线,溶液浓度将_(偏高、偏低、无影响)。
(2)在淀粉碘化钾溶液中通入少量氯气,立即会看到溶液变蓝色,这是因为_______________________________________________(请用化学方程式辅以简要文字进行解释)