(6分)实验探究是科学探究的重要方法,如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题(已知铜粉在加热条件下能与氧气反应生成固体氧化铜).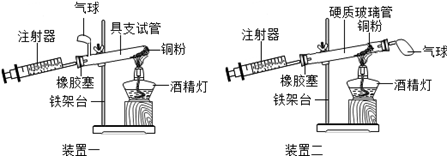
(1)根据下表提供的实验数据,完成下表.
| 硬质玻璃管中空气的体积 |
反应前注射器中空气体积 |
反应后注射器中气体体积 |
实验测得空气中氧气的体积分数 |
| 25mL |
15mL |
9mL |
|
(2)装置一和装置二中气球的位置不同, (填“装置一”或“装置二”)更合理,理由 是 .实验过程中,注射器如何操作? .
(3)若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?(列举两 条) 、 .
已知某纯碱样品中含有NaCl杂质,为测定样品中纯碱的质量分数,可用下图中的装置进行实验(温馨提示:碱石灰的主要成分是NaOH和CaO)。主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将ag样品放入锥形瓶中,加适量蒸馏水溶解,得到样品溶液
③称量盛有碱石灰的U型管的质量,得到bg
④从分液漏斗滴入稀硫酸到不再产生气体为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到cg
⑦重复步骤⑤和⑥的操作,直到盛有碱石灰的U型管的质量基本不变,为dg
请回答下列问题:
(1)在用托盘天平称量样品时,如果天平的指针向右偏转,说明;
(2)装置中
溶液的作用是;
(3)装置中浓硫酸的作用是:
(4)如果将分液漏斗中的稀硫酸换成浓度相同的盐酸,测定的结果会(填偏高、偏低或不变):
(5)步骤⑤的目的是;
(6)该样品中纯碱的质量分数的计算式为:
(4分)化学反应都遵守质量守恒定律,请根据质量守恒定律的相关知识完成下列问题:
(1)下列各项中,在化学反应前后一定不变的是(填数字序号)。
①元素的种类②物质的种类 ③原子的种类
④分子的种类 ⑤原子的数目⑥分子的数目
(2)应用质量守恒定律配平化学方程式:
(3)实验室常用右图所示实验验证质量守恒定律。四位同学设计了如 下A、B、C、D四个实验,并按右图实验操作来验证质量守恒定律,实验中观察到B、C实验前后天平依然保持平衡,某同学认为B、C实验都能验证质量守恒定律,你认为他的说法(填"是"或"否")正确;而A、D实验天平不平衡,其中D实验天平不平衡的原因是。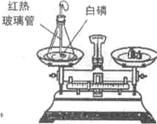

小李和小高同学用一瓶久置的氢氧化钠溶液和稀硫酸做中和反应的实验,为了能够观察到明显现象,他们先向盛装
氢氧化钠溶液的烧杯中滴加几滴酚酞试液,再逐滴滴加稀硫酸并不断搅拌。
(1)滴加稀硫酸的过程中观察到有气泡产生,他们发现氢氧化钠溶液已变质,请你写出氢氧化钠溶液变质的化学方程式:。
(2)他们对该瓶氢氧化钠溶液的变质情况进行探究
【猜想】猜想一:全部变质猜想二:部分变质
【实验探究】他们按下列实验方案进行探究,请你帮他们把下表补充完整:(温馨提示:氯化钡溶液呈中性)
| 实验步骤 |
实验现象 |
实验结论 |
| ①取少量上述氢氧化钠溶液于试管中,然后滴加过量氯化钡溶液,充分反应后过滤。 |
猜想二成立 |
|
| ②向所得溶液液中滴加几滴酚酞试液。 |
【反思与评价】小李认为在上述实验中可用氢氧化钡溶液代替氯化钡溶液,也能证明猜想二成立,你认为(填"可行"或"不可行")。
某化学兴趣小组为了探究铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行了如下探究活动:
【查阅资料】铬(
)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜。铬能与稀硫酸反应,生成氢气和硫酸亚铬(
)。
【提出猜想】对这三种金属的活动性顺序提出了如下猜想:
猜想①:
猜想②:
猜想③: 猜想④:
【讨论交流】根据已学的金属活动性顺序和已查阅的资料分析,肯定不能成立的是猜想是和猜想(填序号)。
【实验设计及过程】请将表中的内容填写完整。
| 实 验 操 作 |
实 验 现 象 |
实 验 结 论 |
| 室温下,将大小相同并打磨光亮的铬片、铝片、铜片分别投入盛有体积相同、相同的稀硫酸的试管中 |
铬片表面产生气泡缓慢;铝片表面产生气泡较快;铜片表面 | 猜想(填序号)成立 |
【实验反思】
(1)将金属片投入稀硫酸前应先打磨金属片的目的是。
| A. |
除去金属表面氧化物,有利于直接反应 |
B. |
使金属表面光亮,便于观察现象 |
C. |
使金属表面温度升高,提高反应温度 |
(2)有同学提出探究金属活动性强弱还可以依据"金属与盐溶液是否发生置换反应"来判断。为了验证甲、乙、丙三种金属的括动性依次减弱,某同学设计了如下方案:
①把甲放入乙的盐溶液中
②把乙放入丙的盐溶液中
③把甲放入丙的盐溶液中
你认为该方案中的(填序号)没有必要做。
某白色固体可能由氢氧化钡(化学式为
)、氢氧化钠中的一种或两种组成。为确定该固体物质的成分,某化学兴趣小组进行下列探究活动,请你认真阅读有关信息,回答相关问题。
【查阅资料】(1)
是一种强碱,具有NaOH相似的化学性质。
(2)部分酸、碱、盐的溶解性如下表所示:
【提出猜想】猜想I :该固体是
猜想Ⅱ:该固体是
猜想Ⅲ:该固体是
、
的混合物
【设计实验】
【问题讨论】
(1)实验步骤①中发生反应的化学方程式为。
(2)实验步骤②得出的实验结论(填"正确"或"不正确")。
(3)如果在上述实验中用稀硫酸代替硫酸钠溶液,实验步骤和实验现象均相同,你可以判断出猜想是成立的。