下列电解质在水中的电离方程式书写错误的是( )
| A.NaHCO3=Na++H++CO32- | B.NaHSO4=Na++H++SO42- |
| C.MgCl2=Mg2++2Cl- | D.Ba(OH)2=Ba2++2OH- |
已知七种短周期元素a~g的有关信息如下表所示:下列推断正确的是
| 元素编号 |
a |
b |
c |
d |
e |
f |
g |
| 原子半径 / nm |
0.037 |
0.074 |
0.082 |
0.102 |
0.143 |
0.152 |
0.186 |
| 最高化合价或最低化合价 |
+1 |
-2 |
+3 |
-2 |
+3 |
+1 |
+1 |
A.氢氧化物碱性的强弱:f < g
B.简单离子的离子半径:b < g
C.元素e的氧化物只能与酸反应
D.元素a与元素d形成的化合物属于离子化合物
下列有关电能特点的说法错误的是
| A.电能是现代社会应用最广泛,使用最方便,污染最小的二次能源; |
| B.目前我国发电总量中火电所占比率最多; |
| C.燃煤发电过程中能量转换方式为:化学能→热能→机械能→电能; |
| D.火力发电过程中能量转化率很高。 |
氢氧燃料电池已用于航天飞机,以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2 + 4OH— - 4e— ="=" 4H2O O2 + 2H2O + 4e— ="=" 4OH—
据此作出判断,下列说法中错误的是
| A.H2在负极发生氧化反应 |
| B.供电时总反应为:2H2 + O2 ="=" 2H2O |
| C.产物为无污染的水,属于环境友好电池 |
| D.燃料电池的能量转化率可达100% |
下列关于充电电池的叙述,不正确的是
| A.充电电池的化学反应原理是氧化还原反应 |
| B.充电电池可以无限制地反复放电、充电 |
| C.充电是使放电时的氧化还原反应逆向进行 |
| D.较长时间不使用电器时,最好从电器中取出电池,并妥善存放。 |
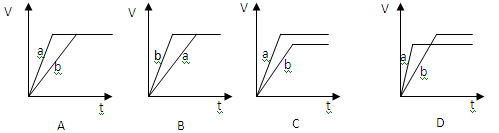
等质量的两份锌粉a和b,分别加入过量的稀硫酸中,并向a中加入少量CuSO4溶液,下图表示产生H2的体积(V)与时间(t)的关系正确的是