一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO2(g)+2CO(g) 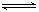 2CO2(g)+S(l) ΔH<0
2CO2(g)+S(l) ΔH<0
若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
| A.平衡前,随着反应的进行,容器内压强始终不变 |
| B.平衡时,其他条件不变,分离出硫,正反应速率加快 |
| C.平衡时,其他条件不变,升高温度可提高SO2的转化率 |
| D.其他条件不变,使用不同催化剂,该反应的平衡常数不变 |
下列关于苯的说法中,正确的是[
| A.苯不能使酸性KMnO4溶液褪色,因而应属于饱和烃 |
B.苯的结构式为 ,分子中含有双键,所以属于烯烃 ,分子中含有双键,所以属于烯烃 |
| C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应 |
| D.苯分子为平面正六边形结构,6个碳原子之间的碳碳键完全相同 |
在某无色透明的酸性溶液中,能大量共存的离子组是
| A.Na+ 、K+、SO42-、HCO3- | B.Na十、Ba2+、NO3-、SO42- |
| C.Na+、 K+、Cl-、 NO3- | D.Fe3+、K+、SO42-、OH- |
下列各组顺序的排列不正确的是
| A.原子半径:Na>Mg>Al>H |
| B.热稳定性: HC l<H2S<PH3 |
| C.酸性强弱:H2SiO3<H2CO3<H3PO4 |
| D.氧化性:K+<Na+<Mg2+<Al3+ |
对于可逆反应2HI(g)  I2(g)+H2(g),下列叙述能够说明已达到平衡状态的是
I2(g)+H2(g),下列叙述能够说明已达到平衡状态的是
| A.各物质的量的浓度比2 : 1 : 1 |
| B.容器内的总压不随时间变化 |
| C.断裂2 mol H-I键的同时生成1 mol I-I键 |
| D.混合气体的颜色不再变化时 |
下图所示的某有机反应,其反应类型为
| A.加成反应 | B.取代反应 | C.酯化反应 | D.置换反应 |