对于可逆反应:2SO2(g)+O2(g) 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
| A.增大压强 | B.升高温度 |
| C.使用催化剂 | D.多充O2 |
可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:
有关该电池的说法正确的是()
| A.放电时负极附近溶液的碱性不变 |
| B.充电过程是化学能转化为电能的过程 |
| C.充电时阳极反应:Ni(OH)2-e— + OH--="=" NiOOH + H2O |
| D.放电时电解质溶液中的OH---向正极移动 |
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A.5.6 g铁与足量盐酸反应转移的电子数为0.3NA |
| B.100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子均为0.2NA |
| C.标准状况下,22.4 L氦气与22.4 L氟气所含原子数均为2 NA |
| D.20 g重水(D2O)中含有的电子数为10NA |
向一定的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是()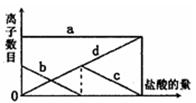
| A.a:Cl—; b:K+; c:CO32—; d:HCO3— |
| B.a:K+; b:CO32—; c:Cl—; d:HCO3— |
| C.a:K+; b:CO32—; c:HCO3—; d:Cl— |
| D.a:K+; b:HCO3—;c:Cl—; d: CO32— |
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是()
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是()
| A.以X浓度变化表示的反应速率为0.001 mol/(L·s) |
| B.将容器体积变为20 L,Z的平衡浓度变为原来的1/2 |
| C.若升高温度Y的转化率减小,则正反应为吸热反应 |
| D.达到平衡时,X与Y 的浓度相等 |
下列反应的离子方程式正确的是()
| A.碳酸氢钙溶液中加入足量的苛性钠溶液:Ca2++HCO3---+OH---=CaCO3↓+H2O |
B.电解饱和食盐水: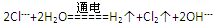 |
| C.氯气通入冷的氢氧化钠溶液中:2Cl2+2OH---=3Cl---+ClO---+H2O |
| D.FeBr2溶液中通入足量的Cl2:2Fe2++Cl2=2Fe3++2Cl--- |