在100 ℃时,把0.5 mol N2O4通入体积为5 L的真空密闭容器中,立即出现红棕色。反应进行到2 s时,NO2的浓度为0.02 mol·L-1。在60 s时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是( )
| A.前2 s以N2O4的浓度变化表示的反应速率为0.01 mol·L-1·s-1 |
| B.在2 s时体系内的压强为开始时的1.1倍 |
| C.在平衡时体系内含N2O4 0.25 mol |
| D.平衡时,N2O4的转化率为40% |
下列有关物质性质、应用的说法正确的是
| A.氯化铝是电解质,可电解其水溶液获得金属铝 |
| B.二氧化硅具有导电性,可用于生产光导纤维 |
| C.SO2具有漂白性,可用于将银耳漂白为“雪耳” |
| D.小苏打可与酸反应,可用作治疗胃酸过多的药剂 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.c(ClO-)=1.0mol·L-1的溶液中:Na+、SO32-、S2-、SO42- |
| B.由水电离的c(H+)=1×10-12 mol·L-1的溶液中:Ba2+、K+、Cl-、NO3- |
| C.常温下,c(H+)/c(OH-)=10-10的溶液中:Ca2+、Mg2+、HCO3-、I- |
| D.滴入少量KSCN溶液显红色的溶液中:Na+、K+、I-、SO42- |
下列有关化学用语表示正确的是
| A.明矾的化学式:KAl(SO4)2 |
B.氯离子的结构示意图: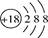 |
C.中子数为10的氧原子: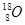 |
D.溴化铵的电子式: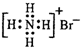 |
化学家认为石油、煤作为能源使用时,燃烧了“未来的原始材料”。下列对上述观点理解正确的是
| A.大力提倡使用廉价化石燃料作为能源 |
| B.化石燃料属于可再生能源,不影响可持续发展 |
| C.应更多地利用石油和煤生产基本化工原料 |
| D.研发新型催化剂,提高石油和煤中各组分的燃烧热 |
向甲、乙两个容积均为1L的恒容容器中,分别充入2molA、2molB和1molA、1molB。相同温度下,发生反应:A(g)+B(g) xC(g)△H<0。测得两容器中c(A)随时间t的变化如图所示
xC(g)△H<0。测得两容器中c(A)随时间t的变化如图所示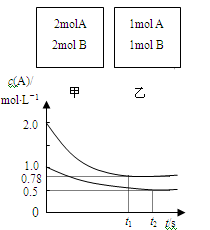
下列说法正确的是
A.x不可能等于2
B.甲、乙两容器中反应达平衡时,平衡常数K(甲) <K(乙)
C.将乙容器升温可使甲、乙容器内各物质的体积分数相同
D.若向甲容器中再充入2molA、2molB,则平衡时甲容器中0.78 mol/L<c(A)<1.56 mol/L