欲配制100 mL 1.0 mol/L Na2SO4溶液,正确的方法是( )
①将14.2 g Na2SO4 溶于100 mL水中
②将32.2 g Na2SO4·10H2O溶于少量水中,再用水稀释至100 mL
③将20 mL 5.0 mol/L Na2SO4溶液用水稀释至100 mL
| A.①② | B.②③ | C.①③ | D.①②③ |
下列图示与对应叙述相符合的是( )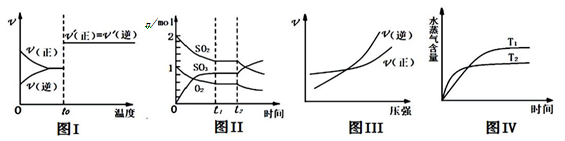
A.图I:反应H2+I2 2HI 达平衡后,升高温度时反应速率随时间的变化 2HI 达平衡后,升高温度时反应速率随时间的变化 |
B.图Ⅱ:反应2SO2+O2 2SO3达平衡后,缩小容器体积时各成分的物质的量随时间的变化 2SO3达平衡后,缩小容器体积时各成分的物质的量随时间的变化 |
C.图III:反应N2+3H 2 2NH3 在恒温情况下,反应速率与压强的关系 2NH3 在恒温情况下,反应速率与压强的关系 |
D.图IV:反应CO2(g)+H2(g) CO(g)+H2O(g)ΔH>0,水蒸气含量随时间的变化 CO(g)+H2O(g)ΔH>0,水蒸气含量随时间的变化 |
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)Y(?) aZ(g)。
aZ(g)。
此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )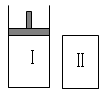
| A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ |
| B.若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ |
| C.a为2 |
| D.平衡时Ⅰ容器的体积小于V L |
某温度下,有反应H2(g)+I2(g)  2HI(g);正反应为放热反应,在带有活塞的密闭容器中达到平衡。下列说法中正确的是( )
2HI(g);正反应为放热反应,在带有活塞的密闭容器中达到平衡。下列说法中正确的是( )
| A.体积不变,升温,正反应速率减小 |
| B.温度、压强均不变,充入HI气体,开始时正反应速率增大 |
| C.温度不变,压缩气体的体积,平衡不移动,颜色加深 |
| D.体积、温度不变,充入氮气后,正反应速率将增大 |
可逆反应2A(g)+3B(g)  2C(g)+D(g)在四种不同条件下的反应速率分别为:①v(A)=0.5 mol/(L·min) ②v(B)=0.6 mol/(L·min) ③v(C)=0.35 mol/(L·min)④v(D)=0.4 mol/(L·min)。则该反应在不同条件下反应速率最快的是( )
2C(g)+D(g)在四种不同条件下的反应速率分别为:①v(A)=0.5 mol/(L·min) ②v(B)=0.6 mol/(L·min) ③v(C)=0.35 mol/(L·min)④v(D)=0.4 mol/(L·min)。则该反应在不同条件下反应速率最快的是( )
A.① B.② C.③D.④
在某一化学反应中,反应物A的浓度在15 s内从3.0 mol/L变成1.5 mol/L,
在这15 s内A的化学反应速率为( )
| A.1.5 mol/(L·s) | B.1.5 mol/L |
| C.0.1 mol/(L·s) | D.0.1 mol/L |