下列离子方程式书写正确的是
A.沸水中滴入FeCl3饱和溶液:Fe3++3H2O Fe(OH)3+3H+ Fe(OH)3+3H+ |
| B.一小块钠投入水中:Na+2H2O=Na++2OH-+H2↑ |
| C.用氢氧化钠溶液吸收过量二氧化碳 OH-+CO2=HCO3- |
| D.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3+ +2I-=2Fe2+ + I2 |
某学生用下图制作了原电池,其中正确的是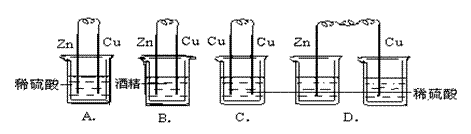
化学反应速率受外界条件的影响很大,下列条件的改变肯定可以加快化学反应速率的措施是
| A.降低压强 | B.改变浓度 | C.升高温度 | D.降低温度 |
一种甲烷水合物晶体中,平均每46个分子构成8个水分子笼,每个水分子笼可容纳1个甲烷分子或水分子,若这8个分子笼中有6个容纳的是甲烷分子,另外2个被水分子填充,这种可燃冰的平均分子组成是
| A.CH4·5H2O | B.CH4·6H2O | C.CH4·7H2O | D.CH4·8H2O |
一定温度下,某一密闭且体积不变的容器内有可逆反应:A(g)+3B(g) 2C(g)。该反应进行到一定限度后达到了化学平衡,该化学平衡的标志是
2C(g)。该反应进行到一定限度后达到了化学平衡,该化学平衡的标志是
A.单位时间内生成amol物质A,同时生成3amol物质B
B.容器内气体的密度不再随时间而改变
C.C物质的生成速率和分解速率相等
D.A、B、C随着物质的分子数之比为1:3:2
煤的气化是煤高技、洁净利用的方向之一;下图为加热某地煤样所得煤气组成及体积分数随温度变化的曲线图。由图可知该煤气中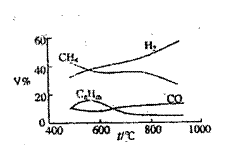
| A.只含有碳、氢两种元素 |
| B.所含的有机物是CH4,CnHm,CO |
| C.CO体积分数小于CH4体积分数 |
| D.氢气体积分数最大 |