用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.0.1mol·L-1的Na2CO3溶液中,阴离子的总数目大于0.1NA |
| B.常温下,46 g NO2和N2O4混合气体中含有的分子总数为2NA |
| C.标准状况下,22.4L的HF含有NA个分子 |
| D.标准状况下,10g的庚烷分子中含有2.2NA个共价键 |
如图表示4-溴环己烯所发生的4个不同反应.其中,产物只含有一种官能团的反应是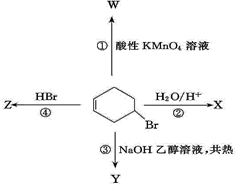
| A.①④ | B.②③ | C.①② | D.③④ |
Cyrneine A对治疗神经系统疾病有着很好的疗效.可用香芹酮经过多步反应合成: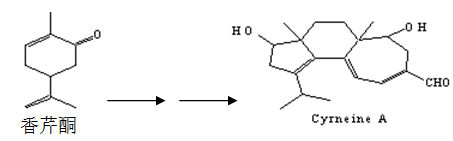
下列说法正确的是
| A.香芹酮化学式为C9H12O |
| B.Cyrneine A可以发生加成反应、氧化反应,但不能发生消去反应 |
| C.香芹酮和Cyrneine A均能使酸性KMnO4溶液褪色 |
| D.与香芹酮互为同分异构体,分子中有4种不同化学环境的氢原子的酚类化合物共有4种 |
研究人员最近发现了一种“水”电池,这种电池能利用淡水和海水之间含盐量的差别进行发电,在海水中电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是
| A.Ag发生还原反应 |
| B.正极反应式:5MnO2+2e- =Mn5O102- |
| C.每生成1mol AgCl转移2mol电子 |
| D.Cl—不断 向“水”电池的正极移动 |
下列说法均摘自学生的作业本,你认为无科学性错误的是
| A.煤的气化、液化都是化学变化,可为人类提供清洁高效的燃料 |
| B.氯化氢、氯气、二氧化氮、生石灰溶于水都有化学键被破坏的变化,都属于化学变化 |
| C.苯酚、纯碱、胆矾和OF2分别属于酸、碱、盐和氧化物 |
| D.二氧化碳、氨气、氯气都是非电解质 |
常温下有碳原子数不超过4的A和B两种气态烃的混合物,已知B的相对分子质量大于A的相对分子质量,则不论A和B以何种比例混合,碳氢质量比总是小于6:1而大于4:1的可能组合有(不考虑同分异构现象)
| A.6种 | B.9种 | C.12种 | D.15种 |