煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s) + CO(g) CaO(s) + SO2(g) + CO2(g) ΔH1=+218.4kJ·mol-1(反应Ⅰ)
CaO(s) + SO2(g) + CO2(g) ΔH1=+218.4kJ·mol-1(反应Ⅰ)
CaSO4(s) + 4CO(g) CaS(s) + 4CO2(g) ΔH2=-175.6kJ·mol-1(反应Ⅱ)
CaS(s) + 4CO2(g) ΔH2=-175.6kJ·mol-1(反应Ⅱ)
假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是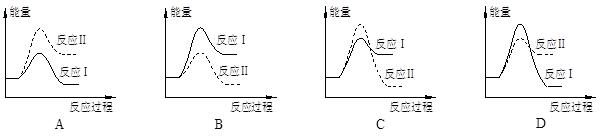
实验室需950mL 2mol/L的碳酸钠溶液,选取容量瓶的规格和称取碳酸钠的质量为
| A.1000mL、212 g | B.950mL、201.4 g |
| C.500mL、286 g | D.任意规格、572 g |
NA代表阿伏加德罗常数,下列说法正确的是
| A.1 mol NaCl固体溶于1 L水所得溶液中NaCl的物质的量浓度为1 mol·L-1 |
| B.2.3 g钠转化为钠离子时失去的电子数目为0.1NA |
| C.常温常压下,11.2 L H2所含的原子数目为NA |
| D.28 g氮气所含的原子数目为NA |
下列化学反应属于氧化还原反应且水既不作氧化剂又不作还原剂的是
| A.CaO + H2O = Ca(OH)2 |
| B.NaH + H2O =" NaOH" + H2↑ |
| C.3NO2 + H2O = 2HNO3 + NO |
| D.2H2O + 2F2 =" 4HF" + O2↑ |
下列物质属于非电解质的是
| A.C2H5OH | B.NaOH | C.NaCl | D.H2SO4 |
焰色反应每次实验都要用试剂洗净铂丝,这种试剂是
| A.Na2CO3溶液 | B.NaOH溶液 | C.硫酸 | D.稀盐酸 |