过氧化氢的沸点比水高,但受热容易分解。某试剂厂先制得7%~8%的过氧化氢溶液,再浓缩成30%的溶液时,可采用的适宜方法是
| A.常压蒸馏 | B.减压蒸馏 | C.加生石灰常压蒸馏 | D.加压蒸馏 |
下列有关铁元素的叙述中正确的是( )
| A.Fe(OH)2易被氧化成Fe(OH)3,说明稳定性: Fe(OH)2<Fe(OH)3 |
| B.铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3 |
| C.氢氧化铁与氢碘酸反应:Fe(OH)3+3HI=FeI3+3H2O |
| D.铁元素位于周期表的第四周期第ⅧB族 |
将一定质量的Mg、Al合金投入2.0 mol/L、250 mL的稀硫酸中,金属全部溶解。然后向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是( )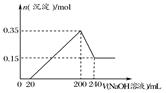
| A.当加入NaOH溶液的体积为20 mL时,溶液的pH等于7 |
| B.当加入NaOH溶液的体积为20 mL时,溶液中的溶质只有硫酸镁和硫酸铝 |
| C.生成的H2在标准状况下的体积为11.2 L |
| D.所加NaOH溶液的物质的量浓度为5.0 mol/L |
下列各组物质中,不是按下图所示(“→”表示一步完成)关系相互转化的是( )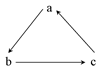
| 选项 |
a |
b |
c |
| A |
Fe |
FeCl3 |
FeCl2 |
| B |
Cl2 |
NaClO |
NaCl |
| C |
Si |
SiO2 |
H2SiO3 |
| D |
HNO3 |
NO |
NO2 |
将1.12 g铁粉加入25 mL 2 mol/L的FeCl3溶液中,充分反应后,其结果是( )
| A.铁有剩余,溶液呈浅绿色,Cl-浓度基本不变 |
| B.向溶液中滴入无色的KSCN溶液,显血红色 |
| C.Fe2+和Fe3+的物质的量之比为5:1 |
| D.氧化产物与还原产物的物质的量之比为2:5 |
相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是( )
| A.Al2O3 | B.Al(OH)3 | C.AlCl3 | D.Al |