已知:①H2O(g)=H2O(l) △H1=-Q1 kJ·mol—1;
②C2H5OH(g)=C2H5OH(l) △H2=-Q2 kJ·mol—1
③C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3 kJ·mol—1
若使23g酒精液体完全燃烧,生成稳定的氧化物,最后恢复到室温,则放出的热量是多少kJ( )
| A.Q1+ Q2+Q3 | B.0.5(Q1+Q2+Q3) |
| C.0.5 Q1-1.5 Q2+0.5Q3 | D.1.5Q1-0.5Q2+0.5Q3 |
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是
| A.②④⑤③① | B.③②④①⑤ | C.③④②⑤① | D.②④③⑤① |
将0.4gNaOH和1.06gNa2CO3混 合并配成溶液,向溶液中滴加0.1mol·L--1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2
合并配成溶液,向溶液中滴加0.1mol·L--1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2 的物质的量的关系是
的物质的量的关系是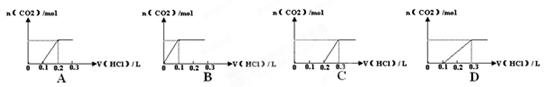
下列各溶液中一定能大量共存的微粒是
| A.常温下,c(H+)= 10—14mol/L的溶液中,Na+、NO3--、Al(OH)4--、CO32-- |
| B.加入Al能产生气泡的溶液中:Fe2+、NO3--、NH4+、Cl-- |
| C.含有大量Al3+的溶液中:Mg2+、Ba2+、F--、I-- |
| D.加入石蕊变红的无色溶液中:Na+、K+、MnO4--、SO42-- |
SO2通入足量Fe(NO3)3稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。针对上述一系列变化过程中,下列说法中不正确的是
| A.上述过程中,最终被还原的是NO3-- |
| B.从上述过程中可以得出结论,氧化性:HNO3>Fe3+>稀H2SO4 |
| C.上述过程中,会产生一种无色无味的难溶于水的气体 |
D.假设通入的SO2完全反应,则同温同压下,S O2和逸出气体的体积为1∶1 O2和逸出气体的体积为1∶1 |
SCl2熔点为—78℃,沸点为59℃。若0.2mol SCln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀。下列判断错误的是
| A.n =" 2" | B.SCln中每个原子最外层均满足8电子稳定结构 |
| C.SCln在固态时为分子晶体 | D.SCln溶于水能电离出Cl-- |