关于下列各装置图的叙述中,不正确的是
| A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+ |
| C.装置③中钢闸门应与外接电源的负极相连 |
| D.装置④中的铁钉几乎没被腐蚀 |
下列说法正确的是(NA为阿伏加德罗常数的值) ()
| A.常温常压下,1.8g D2O中所含的中子数为NA |
| B.标准状况下,2.24L戊烷所含分子数为0.1NA |
| C.常温常压下,0.2mol O2所含原子数为0.2NA |
| D.0.1mol乙醇中含有C-H键的数目为0.5NA |
下列排列顺序正确的是()
①热稳定性:H2O>HF>H2S②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4④结合质子能力:OH->CH3COO->Cl-
| A.①③ | B.②④ | C.①④ | D.②③ |
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。则原溶液中Al3+、Mg2+、NH4+的物质的量分别为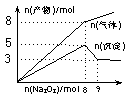
| A.2 mol、3 mol、8 mol | B.3 mol、2 mol、8 mol |
| C.2 mol、3 mol、4 mol | D.3 mol、2 mol、4 mol |
一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通乙烷(C2H6)和氧气,有关此电池的推断错误的是
| A.通乙烷的电极为负极,电极反应为:C2H6+18OH――14e—=2CO32-+12H2O |
B.参加 反应的O2与C2H6的物质的量之比为7∶2 反应的O2与C2H6的物质的量之比为7∶2 |
| C.放电一段时间后,KOH的物质的量浓度将下降 |
D.放电一段时间后,正极 区附近溶液的pH减小 区附近溶液的pH减小 |
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是
| 元素代号 |
A |
B |
D |
E |
G |
H |
I |
J |
| 化合价 |
–1 |
–2 |
+4、–4 |
–1 |
+5、–3 |
+3 |
+2 |
+1 |
| 原子半径/nm |
0.071 |
0.074 |
0.077 |
0.099 |
0.110 |
0.143 |
0.160 |
0.186 |
A.A的单质能将E单质从HE的溶液中置换出来
B.A、H、J的离子半径由大到小顺序是A>J>H
C.G元素的单质不存在同素异形体
D.I在DB2中燃烧生成两种化合物