向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也相应不同。若向M中逐滴加入盐酸,产生气体的体积V(CO2)与加入盐酸的体积V(HCl)的关系分别有下列图示的四种情况,且(2)、(3)、(4)图中分别为:OA<AB,OA=AB,OA>AB。则下列分析与判断正确的是(注:为方便计算与判断,不计CO2的溶解) 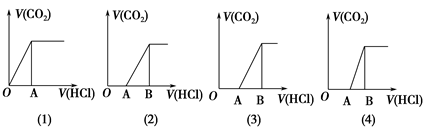
A.M中只有一种溶质的只有(1)
B.M中有两种溶质的有(2)和(4)
C.(2)图显示M中c(NaHCO3)>c(Na2CO3)
D.(4)图显示M中c(NaHCO3)>c(Na2CO3)
制取相同质量的CO2,若要节省酸,可选下列哪种物质()
| A.NaHCO3 | B.Na2CO3 |
| C.CaCO3 | D.K2CO3 |
当金属钠着火时可以用作灭火的物质或器材的是()
| A.水 | B.砂 |
| C.煤油 | D.泡沫灭火器 |
向紫色石蕊试液中加入过量Na2O2粉末,振荡,正确的叙述是()
| A.溶液仍为紫色 | B.最后溶液变蓝色 |
| C.最后溶液褪色 | D.有气泡产生 |
放置于空气中,易发生氧化还原反应而变质的化合物是()
| A.Na2O2 | B.Na2CO3 |
| C.NaHCO3 | D.NaOH |
下列有关热稳定性的强弱比较,不正确的是()
| A.Na2O2>Na2O | B.NaHCO3<Na2CO3 |
| C.KClO3>KCl | D.K2MnO4>KMnO4 |