下列有关化学用语表示正确的是
| A.葡萄糖的结构简式:C6H12O6 |
| B.NaHCO3的电离:NaHCO3=Na++H++CO32- |
C.质子数为53、中子数为78的碘原子: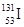 |
D.CO2的电子式: |
有一真空瓶质量为m1,该瓶充入空气后质量为m2。在相同状况下,若改为充入某气体A时,总质量为m3。则A的相对分子质量是()
A.29 |
B.29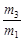 |
C.29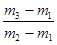 |
D.29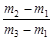 |
设NA为阿伏加德罗常数,下列说法中,正确的是()
| A.2.4 g金属镁所含电子数目为0.2 NA |
| B.16 g CH4所含原子数目为NA |
| C.17 g NH3 所含中子数目为10 NA |
| D.18 g水所含分子数目为NA |
实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
| A.950 mL 111.2 g | B.500 mL 117 g |
| C.1 000 mL 117 g | D.任意规格 111.2 g |
有一份气体样品的质量是14.2 g,体积是4.48 L(标准状况下),该气体的摩尔质量是( )
| A.28.4 | B.28.4 g / mol | C.71 | D.71 g / mol |
一定条件下自然界存在如下反应:14CuSO4+5FeS2+l2H2O==7Cu2S+5FeSO4+12H2SO4,下列说法中不正确的是 ()
| A.CuSO4和FeS2是氧化剂,FeS2是还原剂 |
| B.5 mol FeS2发生反应,有21 mol e—转移 |
| C.Cu2S既是氧化产物又是还原产物 |
| D.产物中的SO42-有一部分是氧化产物 |