室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
| 实验编号 |
起始浓度/(mol · L -1) |
反应后溶液的pH |
|
| c(HA) |
c(KOH) |
||
| ① |
0.1 |
0.1 |
9 |
| ② |
x |
0.2 |
7 |
下列判断不正确的是
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)= 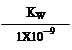 mol · L -1
mol · L -1
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1mol · L -1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)
据以下判断Cu2+、Fe2+、Fe3+的氧化性,从强到弱的顺序为()
① Fe + CuCl2 = FeCl2 + Cu
② 2FeCl3 + Cu = 2FeCl2 + CuCl2
| A.Fe3+>Fe2+>Cu2+ | B.Fe3+>Cu2+>Fe2+ |
| C.Fe2+>Cu2+>Fe3+ | D.Cu2+>Fe2+>Fe3+ |
已知镁和稀硝酸反应时,参加反应的镁和稀硝酸的物质的量之比为2:5 ,此时硝酸的还原产物可能是()
| A.NO2 | B.N2O | C.N2O3 | D.NO |
下列转化过程,需要加入还原剂才能实现的是:( )
| A.CaCO3→CO2 | B.NH4+→NH3 | C.HCl→Cl2 | D.Fe2O3→Fe |
人体血红蛋白中含有Fe2+,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+转变为Fe3+,生成高铁血红蛋白而丧失与氧气结合的能力,服用维生素C可缓解亚硝酸盐中毒,这说明维生素C具有()
| A.酸性 | B.碱性 | C.氧化性 | D.还原性 |
下列各组离子中,能在溶液中大量共存的是()
| A.Na+、Cu2+、Cl-、OH- | B.H+、Ca2+、HCO3-、NO3- |
| C.Fe2+、H+、SO42-、NO3- | D.Na+、CO32-、OH-、K+ |