现有常温下的四种溶液(如下表),下列有关叙述中正确的是( )
| |
① |
② |
③ |
④ |
| 溶液 |
氨水 |
氢氧化钠溶液 |
醋酸溶液 |
盐酸 |
| pH |
11 |
11 |
3 |
3 |
A.分别加水稀释10倍,四种溶液的pH:①>②>④>③
B.温度下降10℃,四种溶液的pH均不变
C.在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变
D.将①、④两种溶液等体积混合,所得溶液中: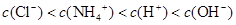
有关常温下pH均为3的醋酸和硫酸的说法正确的是
| A.两种溶液中,由水电离出的氢离子浓度均为1×10-11 mol/L |
| B.分别加水稀释100倍后,两种溶液的pH仍相同 |
| C.醋酸中的c(CH3COO-)和硫酸中的c(SO42-)相等 |
| D.分别加入足量锌片,两种溶液生成H2的体积相同 |
下列说法正确的是( )
| A.向0.1 mol/L Na2CO3溶液中滴加酚酞,溶液变红色 |
| B.Al3+、NO3-、Cl-、CO32-、Na+可大量共存于pH=2的溶液中 |
| C.乙醇和乙酸都能溶于水,都是电解质 |
| D.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同 |
室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。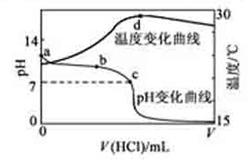
下列有关说法正确的是( )
| A.a点由水电离出的c(H+)=1.0×10-14mol/L |
| B.b点:c(NH4+)+c(NH3·H2O) > c(Cl-) |
| C.c点:c(Cl-)= c(NH4+) |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
下列有关电解质溶液中微粒的物质的量浓度关系错误的是( )
| A.在0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| B.在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3-) |
| C.向0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液: c(CO32-)> c(HCO3-)> c(OH-)>c(H+) |
| D.常温下,CH3COONa和CH3COOH混合溶液[pH=7, c(Na+)=0.1 mol·L-1]: |
c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
常温下用pH为3的某酸溶液分别与pH都为11的氨水、氢氧化钠溶液等体积混合得到a、b两种溶液,关于这两种溶液酸碱性的描述正确的是( )
| A.a不可能显酸性 | B.a可能显酸性或碱性 |
| C.b不可能显碱性 | D.b可能显碱性或酸性 |