下列事实不能用勒夏特列原理解释的是
| A.在硫化氢水溶液中加入碱有利于S2-的生成 |
| B.加入催化剂有利于氨的氧化反应 |
| C.高压有利于合成氨反应 |
| D.向新制氯水中加入碳酸钙有利于次氯酸浓度增大 |
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说法中正确的是
| A.上述四种元素的原子半径大小为W<X<Y<Z |
| B.W与Y可形成既含极性共价键又含非极性共价键的化合物 |
| C.W、X、Y、Z原子的核外最外层电子数的总和为20 |
| D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
可用于电动汽车的铝—空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是
| A.以NaCl溶液或NaOH溶液为电解液时,正极反应式都为:O2+2H2O+4e-===4OH- |
| B.以NaOH溶液为电解液时,负极反应式为Al+3OH--3e-===Al(OH)3 |
| C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变 |
| D.电池工作时,电子通过外电路从正极流向负极 |
下列说法正确的是
| A.镀锌铁和镀锡铁的镀层破损后,前者较易被腐蚀 |
| B.火电是将燃料中的化学能直接转化为电能的过程 |
| C.将煤粉碎了再燃烧可以提高煤的燃烧效率 |
| D.化学反应的限度不可以通过改变条件而改变 |
室温下,将 4 mol A 气体和 2 mol B 气体在 2 L 的密闭容器中混合并在一定条件下发生如下反应:2A(g)+B(g)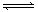 XC(g),经 2 s后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:
XC(g),经 2 s后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:
①用物质 A 表示的反应的平均速率为 0.3 mol/(L·s)
②反应前容器内的压强与平衡后容器内的压强之比为1:1
③ 2 s 时物质A的转化率为30%④ X="2"
其中正确的是
| A.①③④ | B.①④ | C.②③ | D.③④ |
科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:
NaHCO3+H2  HCOONa+H2O下列有关说法正确的是
HCOONa+H2O下列有关说法正确的是
| A.储氢、释氢过程均无能量变化 | B.储氢过程中,NaHCO3被氧化 |
| C.NaHCO3含有离子键和共价键 | D.释氢过程中,每消耗0.1molH2O放出2.24L的H2 |