下图Ⅰ、Ⅱ、Ⅲ分别代表反应①③、②、④,则Y轴是指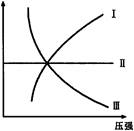
①N2(g)+3H2(g)  2NH3(g);△H=-Q
2NH3(g);△H=-Q
②H2(g)+I2(g)  2HI(g); △H=+Q
2HI(g); △H=+Q
③CO(g)+2H2(g) CH3OH(g); △H=-Q
CH3OH(g); △H=-Q
④2SO3(g)2 2SO2(g)+O2(g); △H=+Q
2SO2(g)+O2(g); △H=+Q
| A.平衡混合气中一种反应物的物质的量 | B.平衡混合气中一种反应物的百分含量 |
| C.平衡混合气中一种生成物的转化率 | D.平衡混合气中一种反应物的转化率 |
下列说法或处理方法不正确的是
| A.焓变是一个反应能否自发进行的相关因素,多数放热反应能自发进行 |
| B.为改善食物的色、香、味并防止变质,可在其中加入一定量的食品添加剂 |
| C.PM2.5与肺癌等疾病的发生有一定的关联 |
| D.塘沽储存危险品仓库着火,消防员立即用大量水和泡沫灭火器进行灭火] |
利用下列装置进行相应实验,不能达到实验目的的是()
| A.①装置可验证酸性:H2CO3>H2SiO3 |
| B.图②装置可用于收集气体H2、CO2、Cl2、NH3 |
| C.图③装置可用于分离互不相溶的两种液体 |
| D.图④装置可制备Fe(OH)2并能较长时间保持其颜色 |
下列事实中,不能用勒夏特列原理加以解释的是
| A.压缩氢气与碘蒸气反应的平衡混合气体,颜色变深 |
B.合成氨反应N2 + 3H2 2NH3△H< 0,为使氨的产率提高,理论上应采取低温高压的措施 2NH3△H< 0,为使氨的产率提高,理论上应采取低温高压的措施 |
| C.向醋酸溶液中加入少量的氢氧化钠固体,CH3COO-离子浓度增加 |
| D.盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,气体颜色变浅 |
下列实验操作、现象及结论均正确的是()
| 选项 |
实验操作 |
现象 |
结论 |
| A |
将SO2通入酸性KMnO4溶液中 |
紫色褪去 |
SO2具有漂白性 |
| B |
用容量瓶配制一定浓度的溶液,定容后摇匀 |
液面低于刻度线 |
溶液浓度偏高 |
| C |
将燃着的镁条伸入盛CO2的集气瓶中 |
镁条继续燃烧 |
镁有较强的还原性 |
| D |
将刚切开的钠块露置在空气中 |
表面变暗 |
钠表面生成Na2O2 |
沼气是一种能源,它的主要成分是CH4,0.5 mol CH4完全燃烧生成CO2和H2O(l)时,放出445 kJ热量,则下列热化学方程式正确的是
A.2CH4(g)+4O2(g) 2CO2(g)+4H2O(l) ΔH="+890" kJ· mol-1 2CO2(g)+4H2O(l) ΔH="+890" kJ· mol-1 |
B.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH="+890" kJ· mol-1 CO2(g)+2H2O(l) ΔH="+890" kJ· mol-1 |
C.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH="-890" kJ· mol-1 CO2(g)+2H2O(l) ΔH="-890" kJ· mol-1 |
D.1/2CH4(g)+O2(g) 1/2CO2(g)+H2O(l) ΔH="-890" kJ· mol-1 1/2CO2(g)+H2O(l) ΔH="-890" kJ· mol-1 |